题目内容
9.1.92gCu投入到一定量浓HNO3中,铜完全溶解,生成的气体颜色由深变成浅(不考虑2NO2?N2O4),共收集到672mL气体(标况),通入一定体积的O2恰好使气体完全溶于水,求通入O2的体积(标况).分析 已知HNO3$\stackrel{Cu}{→}$NO、NO2$\stackrel{O_{2}}{→}$HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,结合电子守恒可知,Cu失去电子数目等于O2得到电子的数目,以此进行计算.
解答 解:n(Cu)=$\frac{1.92g}{64g/mol}$=0.03mol,反应时失去电子数目为2×0.03mol=0.06mol,
反应整个过程为HNO3$\stackrel{Cu}{→}$NO、NO2$\stackrel{O_{2}}{→}$HNO3,反应前后HNO3的物质的量不变,而化合价变化的只有铜和氧气,则Cu失去电子数目等于O2得到电子的数目,所以消耗氧气的物质的量为
n(O2)=$\frac{0.06mol}{4}$=0.015mol,V(O2)=0.015mol×22400ml/mol=336mL,所以通入O2的体积为336mL,
答:应通入O2336mL.
点评 本题考查氧化还原反应的计算,为高频考点,把握发生的反应及电子守恒为解答的关键,侧重分析与计算能力的考查,注意守恒法的应用,题目难度不大.

练习册系列答案
相关题目
20.化学与生活、生产密切相关.下列生活、生产中使用的化学品的溶液能够使pH试纸变蓝.且原因是水解引起的是( )
| A. | 烧碱 | B. | 食用醋 | C. | 氯化铵 | D. | 纯碱 |
17.苯甲酸钠(NaA)可用作饮料的防腐剂,研究表明苯甲酸(HA)的抑菌能力显著高于A-,在生产碳酸饮料的过程中,除了添加NaA外,还需加压冲入CO2气体,已知25℃时,HA、H2CO3的电力平衡常数分别为K=6.25×10-5、K1=4.3×10-7,下列说法正确的是(不考虑饮料中其他成分)( )
| A. | 提高CO2充气压力,饮料中c(A-)不变 | |
| B. | 当pH为5.0时,饮料中 $\frac{c(HA)}{c({A}^{-})}$=0.16 | |
| C. | 相比于未充CO2的饮料,碳酸饮料的抑菌能力较低 | |
| D. | 结合H+的能力:A->HCO3- |
4.在相同条件下,密封容器中气体的分子数与表现出的压强成正比.若将m克焦炭与n克氧气同时放入一密封容器中,测得压强为p1;在一定条件下,当容器内物质充分发生反应后,恢复到原温度时,测得压强为p2.若p1=p2,则两者的质量之比m:n应满足的关系最准确的是( )
| A. | 等于3:8 | B. | 大于3:8 | C. | 小于或等于3:8 | D. | 大于3:4 |
1.元素的性质包含金属性和非金属性,其强弱可以通过该元素对应的某些化学性质体现出来.某同学认为铝元素是金属元素,但是有一定的非金属性.下列化学反应中,你认为能证明铝有非金属性的是( )
| A. | 铝片与盐酸反应生成氢气 | B. | 氢氧化铝溶于强碱溶液 | ||
| C. | 氢氧化铝溶于强酸溶液 | D. | 铝热反应 |
18.在1mol/L CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+,要使溶液pH下降,可采取( )
①加NaOH(s)②加水③加CH3COOH④加CH3COONa(s)⑤加CaCO3(s)⑥加HCl(g)
①加NaOH(s)②加水③加CH3COOH④加CH3COONa(s)⑤加CaCO3(s)⑥加HCl(g)
| A. | ①④ | B. | ③⑥ | C. | 只有② | D. | 只有⑤ |
16.利用硫酸渣(主要含Fe2O3、SiO2、Al2O3、MgO等杂质)制备氧化铁的工艺流程如下:
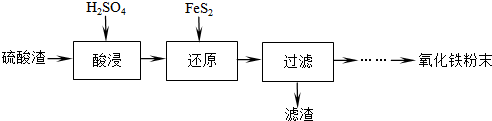
(1)“酸浸”中硫酸要适当过量,目的是提高铁的浸出率,抑制Fe3+的水解.
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO42-+16H+.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量.实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定.有关反应的化学方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-;
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
滴定时,K2Cr2O7标准溶液应盛放在酸式滴定管中(填“酸式”、“碱式”);若不加HgCl2,则测定的Fe3+量偏高(填“偏高”、“偏低”或“不变”).
(4)①可选用KSCN(填试剂)检验滤液中含有Fe3+,产生Fe3+的原因是4Fe2++O2+4H+=4Fe3++2H2O(用离子方程式表示).
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
实验可选用的试剂有:稀硝酸、Ba(NO3)2溶液、酸性KMnO4溶液、NaOH溶液,要求制备过程中不产生有毒气体.请完成由“过滤”后的溶液模拟制备氧化铁的实验步骤:
a.氧化:向溶液中加入过量的酸性高锰酸钾溶液,搅拌.
b.沉淀:滴加NaOH溶液,调节溶液为pH为3.2~3.8.
c.分离,洗涤.
d.烘干,研磨.

(1)“酸浸”中硫酸要适当过量,目的是提高铁的浸出率,抑制Fe3+的水解.
(2)“还原”是将Fe3+转化为Fe2+,同时FeS2被氧化为SO42-,该反应的离子方程式为14Fe3++FeS2+8H2O=15Fe2++2SO42-+16H+.
(3)为测定“酸浸”步骤后溶液中Fe3+的量以控制加入FeS2的量.实验步骤为:准确量取一定体积的酸浸后的溶液于锥形瓶中,加入HCl、稍过量SnCl2,再加HgCl2除去过量的SnCl2,以二苯胺磺酸钠为指示剂,用K2Cr2O7标准溶液滴定.有关反应的化学方程式如下:
2Fe3++Sn2++6Cl-=2Fe2++SnCl62-;
Sn2++4Cl-+2HgCl2=SnCl62-+Hg2Cl2↓
6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
滴定时,K2Cr2O7标准溶液应盛放在酸式滴定管中(填“酸式”、“碱式”);若不加HgCl2,则测定的Fe3+量偏高(填“偏高”、“偏低”或“不变”).
(4)①可选用KSCN(填试剂)检验滤液中含有Fe3+,产生Fe3+的原因是4Fe2++O2+4H+=4Fe3++2H2O(用离子方程式表示).
②已知部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| 完全沉淀 | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
a.氧化:向溶液中加入过量的酸性高锰酸钾溶液,搅拌.
b.沉淀:滴加NaOH溶液,调节溶液为pH为3.2~3.8.
c.分离,洗涤.
d.烘干,研磨.