题目内容
11.用图提供的装置与试剂,组装一套CO还原CuO的实验装置,并回答问题.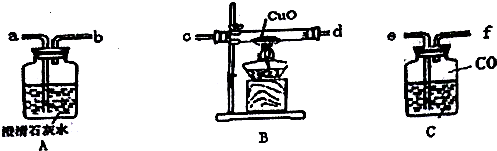
(1)使用CO气体进行实验时,可将水重新注入装置C中而将CO气体排出,此时水应从接口e(填“e”或“f”)流入,实验时气体则依次通过f→c→d→a(填接口处字母);
(2)实验开始时应该先通入一氧化碳,后进行加热反应,原因是CO有可燃性,不纯易发生爆炸;
(3)写出B处发生反应的化学方程式CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
分析 组装一套CO还原CuO的实验装置,则将水重新注入装置C中而将CO气体排出,从长导管注入水,CO从f口出,然后连接c,d连接a,石灰水变浑浊可知生成CO2,因CO不纯时加热可能发生爆炸,则先通入CO排出空气后,再加热,以此来解答.
解答 解:组装一套CO还原CuO的实验装置,则将水重新注入装置C中而将CO气体排出,从长导管注入水,CO从f口出,然后连接c,d连接a,石灰水变浑浊可知生成CO2,因CO不纯时加热可能发生爆炸,则先通入CO排出空气后,再加热,
(1)由上述分析可知,使用CO气体进行实验时,可将水重新注入装置C中而将CO气体排出,此时水应从接口e流入,实验时气体则依次通过f→c→d→a,
故答案为:e;f;a;
(2)实验开始时应该先通入一氧化碳,后进行加热反应,原因是CO有可燃性,不纯易发生爆炸,
故答案为:通入一氧化碳;进行加热反应;CO有可燃性,不纯易发生爆炸;
(3)B处发生反应的化学方程式为CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2,故答案为:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
点评 本题考查性质实验方案的设计,为高频考点,把握物质的性质、发生的反应、实验装置的作用为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
1.我国首创的海洋电池以铝板为负极,铂网为正极,海水为电解质溶液,空气中的氧气与铝反应产生电流.电池总反应为4Al+3O2+6H2O=4Al(OH)3,下列说法错误的是( )
| A. | 负极是铝失电子被氧化 | |
| B. | 电池工作时,电流由铝电极沿导线流向铂电极 | |
| C. | 以网状的铂为正极,可增大与氧气的接触面积 | |
| D. | 该电池通常只需更换铝板就可继续使用 |
2.下列离子方程式书写正确的是( )
| A. | 钠与水的反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 碳酸钙溶于稀醋酸:CaCO3+2H +=Ca2++H2O+CO2↑ | |
| C. | 氢氧化钠溶液中通入过量二氧化碳:OH-+CO2=HCO3- | |
| D. | 向碳酸氢铵稀溶液中加入过量烧碱溶液:NH4++OH-=NH3•H2O |
19.下列不存在丁达尔效应的分散系是( )
| A. | 雾 | B. | 淀粉溶液 | C. | 食盐水 | D. | 氢氧化铁胶体 |
3.关于硫和氧的性质叙述正确的是( )
| A. | 硫在O2中燃烧生成SO2 | B. | 硫在O2中燃烧生成SO3 | ||
| C. | 硫的非金属性比氧的强 | D. | 氧、硫均只有氧化性 |
20.下列关于0.5molO2的说法不正确的是( )
| A. | 含有0.5个氧分子 | B. | 摩尔质量是32g/mol | ||
| C. | 含有3.01×1023个氧分子 | D. | 质量是16g |
1.下列关于弱电解质的电离平衡常数的叙述中,正确的是( )
| A. | 因为电离过程是吸热过程,所以温度越高,同一弱电解质的电离平衡常数越大,电离度越小 | |
| B. | 弱电解质的电离平衡常数是由各微粒的平衡浓度表达的,所以弱电解质的电离平衡常数只与浓度有关 | |
| C. | 对于不同的弱酸,电离平衡常数越大,酸性一定越强,可以通过电离平衡常数的大小判断弱酸的相对强弱 | |
| D. | 弱电解质的电离平衡常数是衡量弱电解质电离程度大小的一种方法 |