题目内容
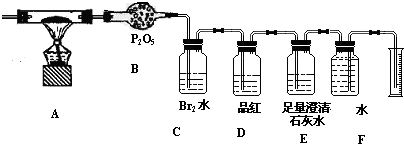
短周期主族元素A、B、C、D、E的原子序数依次增大,它们的原子核外层数之和为10;B的化合物种类繁多,数目庞大.C、D是空气中含量最多的两种元素;D、E两单质可以生成两种不同的离子化合物.X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,某温度下在恒容密闭容器中相互转化时的量变关系如图1:
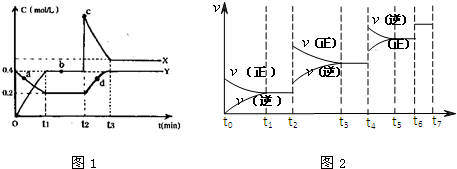
(1)(Ⅰ)X的化学式是 .
(Ⅱ)图中a、b、c、d四点中,表示反应处于平衡状态的是 .
(Ⅲ) 反应进行到t2时刻,改变的条件可能是 ,在t3时重新达到平衡后,与t2时刻相比,X的物质的量浓度 ,X的体积分数 .(填“增大”或“减小”或“不变”)
(2)达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2.图中t4时引起平衡移动的条件是 ;图中表示平衡混合物中X的含量最高的一段时间是 .

(1)(Ⅰ)X的化学式是
(Ⅱ)图中a、b、c、d四点中,表示反应处于平衡状态的是
(Ⅲ) 反应进行到t2时刻,改变的条件可能是
(2)达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2.图中t4时引起平衡移动的条件是
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:B元素的化合物种类繁多,数目庞大,B为C元素;C、D两种元素形成的单质是空气中含量最多的物质,为O2和N2,根据原子序数依次增大,则C为N元素、D为O元素;D、E两元素可以生成两种不同的离子化合物,则E为Na元素;它们原子核外的电子层数之和为10,则A原子电子层数=10-2-2-2-3=1,则A为H元素,
(1)(Ⅰ)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,这两种物质是NO2、N2O4,根据X、Y浓度变化确定这两种物质分别是什么;
(Ⅱ)化学反应达到平衡状态时,各种物质的浓度、百分含量不变;
(Ⅲ)根据图象知X、Y浓度是否变化来确定改变条件;
(2)根据二氧化氮与四氧化二氮的可逆反应特点及影响可逆反应因素进行判断图中t4时引起平衡移动的条件、X的含量最高的一段时间.
(1)(Ⅰ)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,这两种物质是NO2、N2O4,根据X、Y浓度变化确定这两种物质分别是什么;
(Ⅱ)化学反应达到平衡状态时,各种物质的浓度、百分含量不变;
(Ⅲ)根据图象知X、Y浓度是否变化来确定改变条件;
(2)根据二氧化氮与四氧化二氮的可逆反应特点及影响可逆反应因素进行判断图中t4时引起平衡移动的条件、X的含量最高的一段时间.
解答:
解:B元素的化合物种类繁多,数目庞大,B为C元素,C、D两种元素形成的单质是空气中含量最多的物质,为O2和N2,根据原子序数依次增大,则C为N元素,D为O元素,D、E两元素可以生成两种不同的离子化合物,则E为Na元素,它们原子核外的电子层数之和为10,则A原子电子层数为:10-2-2-2-3=1,则A为H元素,
(1)(Ⅰ)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,这两种物质为:NO2、N2O4,
当Y的浓度减少0.2mol/L时,X的浓度增大0.4mol/L,同一时间段、同一化学反应中,物质的量浓度的变化量之比等于其计量数之比,所以X的计量数是2、Y的计量数是1,则X的化学式为NO2,
故答案为:NO2;
(Ⅱ)化学反应达到平衡状态时,各种物质的浓度不变,根据图象知,b点表示平衡状态,
故答案为:b;
(Ⅲ)根据图象知,t2时刻,X浓度增大、Y浓度不变,所以改变的条件是增大NO2的浓度;
由于增大了二氧化氮的浓度,相当于增大了压强,平衡向着正向移动,则在t3时重新达到平衡后,与t2时刻相比,X的体积分数减小,但是由于容器体积缩小,则X的物质的量浓度增大,
故答案为:增大NO2的浓度;增大;减小;
(2)t2~t3段正逆速率都加快,且v(正)>v(逆),平衡正向移动,t4~t5段正逆速率都加快,且v(正)<v(逆),平衡逆向移动,该反应为体积减小的放热反应,若升高温度,平衡逆向移动,若增大压强,平衡正向移动,故t2~t3段为增大压强,t4~t5段为升高温度;
t4~t5段升高温度后,平衡向着逆向移动,NO2的含量增大,所以在t5~t6平衡时NO2的含量达最高,
故答案为:升高温度;t5~t6.
(1)(Ⅰ)X、Y是均由C、D两元素组成的化合物,且C、D在X、Y中的价态相同,这两种物质为:NO2、N2O4,
当Y的浓度减少0.2mol/L时,X的浓度增大0.4mol/L,同一时间段、同一化学反应中,物质的量浓度的变化量之比等于其计量数之比,所以X的计量数是2、Y的计量数是1,则X的化学式为NO2,
故答案为:NO2;
(Ⅱ)化学反应达到平衡状态时,各种物质的浓度不变,根据图象知,b点表示平衡状态,
故答案为:b;
(Ⅲ)根据图象知,t2时刻,X浓度增大、Y浓度不变,所以改变的条件是增大NO2的浓度;
由于增大了二氧化氮的浓度,相当于增大了压强,平衡向着正向移动,则在t3时重新达到平衡后,与t2时刻相比,X的体积分数减小,但是由于容器体积缩小,则X的物质的量浓度增大,
故答案为:增大NO2的浓度;增大;减小;
(2)t2~t3段正逆速率都加快,且v(正)>v(逆),平衡正向移动,t4~t5段正逆速率都加快,且v(正)<v(逆),平衡逆向移动,该反应为体积减小的放热反应,若升高温度,平衡逆向移动,若增大压强,平衡正向移动,故t2~t3段为增大压强,t4~t5段为升高温度;
t4~t5段升高温度后,平衡向着逆向移动,NO2的含量增大,所以在t5~t6平衡时NO2的含量达最高,
故答案为:升高温度;t5~t6.
点评:本题考查了位置结构性质的相互关系及应用,涉及化学平衡、热化学反应方程式的书写、盐类水解等知识点,根据原子结构、元素的含量等知识点来确定元素,再结合外界条件对化学平衡的影响、化学平衡常数的计算等知识点来分析解答,题目难度中等.

练习册系列答案
相关题目
为了保护臭氧层,可采取的有效措施是( )
| A、减少二氧化硫的排放 |
| B、减少卤代烃的排放 |
| C、减少废气的含铅量 |
| D、减少二氧化碳的排放 |
质量相同的乙烯和一氧化碳具有相同的( )
| A、物质的量 | B、原子个数 |
| C、体积和密度 | D、燃烧产物 |
根据下列化学实验示意图,能得出正确结论的是( )
A、 配置一定浓度的烧碱溶液 |
B、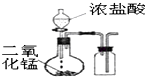 制取并收集Cl2 |
C、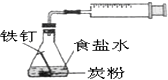 铁的析氢腐蚀 |
D、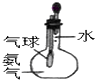 验证氨气易溶于水 |