题目内容
设阿伏加德罗常数为NA,下列叙述中正确的是( )
| A、2NA个HF分子所占的体积约为44.8L |
| B、常温常压下,8.8g CO2和N2O混合气体中所含的电子数为4.4NA |
| C、46g四氧化二氮和二氧化氮的混合气体中含有的原子数少于3NA |
| D、5.6g铁与500mL 2mol?L-1硝酸反应,转移的电子数为0.2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.没有告诉在标况下,且标况下氟化氢也不是气体;
B.CO2和N2O的摩尔质量都是44g/mol,二者分子中都含有22个电子;
C.二氧化氮与四氧化二氮的转化过程中,含有的原子数不变;
D.计算出铁与硝酸的物质的量,根据过量情况判断反应产物及转移的电子数.
B.CO2和N2O的摩尔质量都是44g/mol,二者分子中都含有22个电子;
C.二氧化氮与四氧化二氮的转化过程中,含有的原子数不变;
D.计算出铁与硝酸的物质的量,根据过量情况判断反应产物及转移的电子数.
解答:
解:A.2NA个HF分子的物质的量为2mol,标况下氟化氢不是气体,也没有告诉在标况下,题中条件无法计算2mol氟化氢的体积,故A错误;
B.CO2和N2O的摩尔质量相同,都是44g/mol,则8.8gCO2和N2O的物质的量为:
=0.2mol,二者都含有22个电子,则0.2mol混合气体中含有的电子的物质的量为:22×0.2mol=4.4mol,混合气体中所含的电子数为4.4NA,故B正确;
C.46g四氧化二氮和二氧化氮的混合气体中含有1mol最简式NO2,含有3mol原子,含有的原子数为3NA,故C错误;
D.5.6g铁的物质的量为:
=0.1mol,500mL 2mol?L-1硝酸溶液中含有硝酸的物质的量为:2mol/L×0.5mol=1mol,硝酸过量,0.1mol铁完全反应生成0.1mol铁离子,失去0.3mol电子,转移的电子数为0.3NA,故D错误;
故选B.
B.CO2和N2O的摩尔质量相同,都是44g/mol,则8.8gCO2和N2O的物质的量为:
| 8.8g |
| 44g/mol |
C.46g四氧化二氮和二氧化氮的混合气体中含有1mol最简式NO2,含有3mol原子,含有的原子数为3NA,故C错误;
D.5.6g铁的物质的量为:
| 5.6g |
| 56g/mol |
故选B.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
核内中子数为a的R2+粒子,其核外电子数为b,则该粒子的质量数为( )
| A、2a | B、a+b |
| C、a+b-2 | D、a+b+2 |
下列说法正确的是( )
| A、决定反应速率快慢的因素是催化剂 |
| B、锌粉与稀硫酸反应时,加入少量铜粉能加快产生氢气的速率 |
| C、镁与稀盐酸反应时,加入少量水能加快产生氢气的速率 |
| D、已知:2SO2(g)+O2(g)?2SO3(g)△H=-197 kJ/mol,则2molSO2与 1molO2反应能放出197kJ热量 |
Ba(OH)2溶液滴入KAl(SO4)2溶液中,使SO42-全部转化成BaSO4沉淀,此时铝元素的主要存在形式是( )
| A、Al3+ |
| B、Al(OH)3 |
| C、AlO2- |
| D、Al3+和Al(OH)3 |
从下列事实,找出不能用勒沙特列原理解释的是( )
| A、在溴水中存在如下平衡:Br2+H2O═HBr+HBrO,当加入NaOH溶液后颜色变浅 |
| B、反应CO+NO2?CO2+NO+Q升高温度使平衡向逆方向移动 |
| C、对2HI?H2+I2(气)平衡体系增加压强使颜色变深 |
| D、合成氨反应:N2+3H2?2NH3+Q,为使氨的产率提高,理论上应采取低温 高压的措施 |
化学是一门实用性的学科,以下叙述正确的是( )
| A、.新型能源生物柴油和矿物油主要化学成分相同 |
| B、.“洁厕灵”有效成分为盐酸,与漂白粉混合使用效果更佳 |
| C、静置后的淘米水能产生丁达尔现象,这种“淘米水”是胶体 |
| D、.铝热反应中可得到铁,工业上可以利用该反应来大量生产铁 |
下列有关纯碱的说法正确的是( )
| A、纯碱难溶于水 |
| B、纯碱是碱而不是盐 |
| C、纯碱既可从内陆盐湖提取,又可用“侯氏联合制碱法”生产 |
| D、纯碱中含有少量的小苏打可以用稀盐酸除去 |
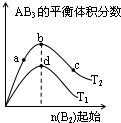 某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )
某化学小组研究在其他条件不变时,改变密闭容器中某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的曲线(图中T表示温度,n表示物质的量)下列判断正确的是( )| A、若T2>T1,则正反应一定是放热反应 |
| B、达到平衡时A2的转化率大小为:b>a>c |
| C、若T2>T1,达到平衡时b、d点的反应速率为vd>vb |
| D、在T2和n(A2)不变时达到平衡,AB3的物质的量大小为:c>b>a |
采用下列装置和操作,不能达到实验目的是( )
A、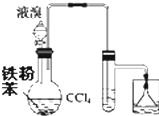 制溴苯并检验HBr |
B、 制乙炔 |
C、 检查装置气密性 |
D、 比较醋酸、碳酸、苯酚酸性强弱 |