题目内容
13.在门窗紧闭的室内用煤炉取暖易发生煤气中毒.引起煤气中毒的主要气体是( )| A. | CO2 | B. | O2 | C. | CO | D. | N2 |
分析 根据煤气中毒即一氧化碳中毒,一氧化碳能与血红蛋白结合,使氧气丧失与血红蛋白结合的机会进行解答.
解答 解:煤气中毒即一氧化碳中毒.一氧化碳是一种无色无味的气体,不易察觉.血液中血红蛋白与一氧化碳的结合能力比与氧的结合能力要强200多倍,从而使氧气丧失与血红蛋白结合的机会,使人缺氧中毒.
故选:C.
点评 本题考查了CO的毒性以及人体中毒原理,题目难度不大,解决的关键是知道一氧化碳中毒的反应机理.

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目
3.美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如图.
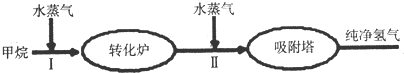
(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的化学平衡常数表达式为K=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$;反应的平衡常数随温度的变化如表:
从表中可以推断:此反应是放(填“吸”、“放”)热反应.在830℃下,若开始时间向恒容密闭容器中充入CO与H2O均为1mol,则达到平衡后CO的转化率为50%.
(2)此流程的第Ⅱ步反应CO(g)+H2O(g)?H2(g)+CO2(g),在830℃,以表格的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有B(填实验编号)
(3)如图表示第Ⅱ步反应的速率(v)随时间(t)变化的关系,下列说法中正确的是A.

A.t2时加入了催化剂 B.t3时降低了温度 C.t3时增大了压强.

(1)此流程的第Ⅱ步反应为:CO(g)+H2O(g)?H2(g)+CO2(g),该反应的化学平衡常数表达式为K=$\frac{c(C{O}_{2})c({H}_{2})}{c(CO)c({H}_{2}O)}$;反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
(2)此流程的第Ⅱ步反应CO(g)+H2O(g)?H2(g)+CO2(g),在830℃,以表格的物质的量(单位为mol)投入恒容反应器发生上述反应,其中反应开始时,向正反应方向进行的有B(填实验编号)
| 实验编号 | n(CO) | n(H2O) | n(H2) | n(CO2) |
| A | 1 | 5 | 2 | 3 |
| B | 2 | 2 | 1 | 1 |
| C | 0.5 | 2 | 1 | 1 |

A.t2时加入了催化剂 B.t3时降低了温度 C.t3时增大了压强.
1.根据下列物质的名称(俗名)写出相应的化学式.
(1)二氧化碳:CO2; (2)硫粉:S;(3)亚硫酸:H2SO3;
(4)氢氧化钙:Ca(OH)2;(5)纯碱:Na2CO3;(6)氧化铝:Al2O3.
(1)二氧化碳:CO2; (2)硫粉:S;(3)亚硫酸:H2SO3;
(4)氢氧化钙:Ca(OH)2;(5)纯碱:Na2CO3;(6)氧化铝:Al2O3.
18.反应A(g)+3B(g)?2C(g)+2D(g),在四种不同情况下的反应速率,其中反应速率最大的是( )
| A. | v(D)=24mol•L-1•min-1 | B. | v(C)=0.5mol•L-1•s-1 | ||
| C. | v(B)=30mol•L-1•min-1 | D. | v(A)=0.15 mol•L-1•s-1 |


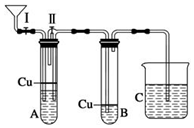 某化学课外兴趣小组为探究NO气体易被空气氧化,并观察NO气体的实际颜色,同时为了防止气体扩散污染空气,对实验室制取NO气体的装置改装如下:
某化学课外兴趣小组为探究NO气体易被空气氧化,并观察NO气体的实际颜色,同时为了防止气体扩散污染空气,对实验室制取NO气体的装置改装如下: