题目内容
新制氯水中存在的微粒是( )
| A、Cl2、HClO |
| B、Cl、Cl-、Cl2 |
| C、Cl2Cl- H+ ClO- H2O和极少量OH- |
| D、Cl2Cl- H+ HClO ClO- H2O和极少量OH- |
考点:氯气的化学性质
专题:卤族元素
分析:氯水中溶解氯气为黄绿色,氯气与水发生:Cl2+H2O?HClO+HCl,溶液中含有Cl2、HClO、H2O等分子,含有H+、ClO-、Cl-等离子,以此解答.
解答:
解:新制氯水溶解氯气为黄绿色,氯气与水发生:Cl2+H2O?HClO+HCl,HClO为弱电解质,存在部分电离,则溶液中含有Cl2、HClO、H2O等分子,含有H+、ClO-、Cl-等离子,
故选D.
故选D.
点评:本题考查氯气的性质,侧重于氯水的成分与性质的考查,为高考高频考点,很好地考查学生的科学素养,能提高学生学习的积极性,难度不大,注意相关基础知识的积累,本题中要注意氯水的成分和性质.

练习册系列答案
相关题目
下列有关化学实验的描述中正确的是( )
| A、分离乙醇和乙酸要用分液的方法 |
| B、配制一定物质的量浓度的NaCl溶液,如果NaCl固体中含有Na2CO3,所配制溶液中c(Na+)将偏高 |
| C、某无色溶液中加稀硫酸产生无色无味气体,该气体能使澄清石灰水变浑浊,说明该溶液中含CO32- |
| D、用苯萃取溴水中的溴时,将溴的苯溶液从分液漏斗下口放出 |
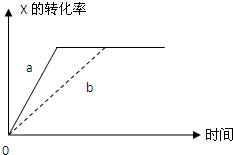 在图中,曲线a表示一定条件下,可逆反应X(g)+Y(g)?2Z(g)+W(s)(正反应放热)的反应过程,若使b曲线变为a曲线,可采取的措施是( )
在图中,曲线a表示一定条件下,可逆反应X(g)+Y(g)?2Z(g)+W(s)(正反应放热)的反应过程,若使b曲线变为a曲线,可采取的措施是( )| A、加催化剂 |
| B、增大Y的浓度 |
| C、降低温度 |
| D、减小反应体系压强 |
有一种气体在标准状况下体积是4.48升,质量是14.2g,则该气体的摩尔质量是( )
| A、28.4 |
| B、28.4g?mol-1 |
| C、71 |
| D、71g?mol-1 |
下列说法正确的是( )
A、钾(K)原子基态的原子结构示意图为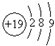 |
B、H2O电子式为 |
| C、Mg的原子基态电子排布式为1s22s22p63s23p1 |
| D、Ca原子基态电子排布式为1s22s22p63s23p6 |
右图是可逆反应A+2B?2C+3D的化学反应速率与化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可以推断( )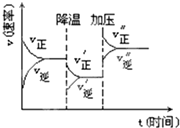

| A、A、B、C、D均为气体 |
| B、若A、B是气体,则C是液体或固体 |
| C、逆反应是放热反应 |
| D、正反应是放热反应 |
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
| A、常温常压下,48g O3所含的氧原子数为 3NA |
| B、常温常压下,22.4 L氧气所含的原子数为 2NA |
| C、标准状况下,22.4L H2O含有的分子数为 NA |
| D、物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl- 个数为 NA |
能用勒沙特列原理解释的是( )
| A、500℃左右比室温更有利于合成氨的反应 |
| B、低压有利于合成氨的反应 |
| C、SO2催化氧化成SO3的反应,往往需要使用催化剂 |
| D、实验室常用排饱和食盐水的方法收集氯气 |