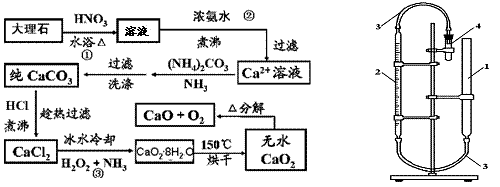
题目内容
| |||||||||||
答案:
解析:
解析:
(1) |
坩埚,样品连续两次高温煅烧,冷却称量质量相差0.1g以内, 在干燥器中冷却,防止CaO冷却的时候吸收空气中的水和CO2. |
(2) |
错误,无论是否发生该反应,生成的CO2的量一定,由C守衡计算出CaCO3的质量一定 |

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目