题目内容
下列表达方式错误的是( )
A、碳-12原子构成
| ||
B、CO2的分子模型示意图: | ||
| C、S2-的核外电子排布式 1s22s22p63s23p6 | ||
D、甲烷的电子式 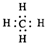 |
考点:电子式、化学式或化学符号及名称的综合
专题:化学用语专题
分析:A.元素符号的左上角表示的是质量数、左下角表示的是质子数;
B.二氧化碳分子中存在两个碳氧双键,为直线型结构;
C.硫离子含有3个电子层,核外电子总数为18,最外层达到8电子稳定结构;
D.甲烷为共价化合物,分子中存在4个碳氢键,碳原子最外层8个电子、H原子最外层2个电子.
B.二氧化碳分子中存在两个碳氧双键,为直线型结构;
C.硫离子含有3个电子层,核外电子总数为18,最外层达到8电子稳定结构;
D.甲烷为共价化合物,分子中存在4个碳氢键,碳原子最外层8个电子、H原子最外层2个电子.
解答:
解:A.碳元素的质子数为6,碳-12原子可以表示为:
C,故A正确;
B.二氧化碳分子为直线型结构,碳原子比较大于氧原子,二氧化碳正确的比例模型为: ,故B错误;
,故B错误;
C.硫离子核外含有3个电子层,最外层达到8电子稳定结构,S2-的核外电子排布式为:1s22s22p63s23p6,故C正确;
D.甲烷分子中含有4个碳氢共用电子对,碳原子最外层达到8电子稳定结构,甲烷的电子式为: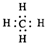 ,故D正确;
,故D正确;
故选B.
12 6 |
B.二氧化碳分子为直线型结构,碳原子比较大于氧原子,二氧化碳正确的比例模型为:
 ,故B错误;
,故B错误;C.硫离子核外含有3个电子层,最外层达到8电子稳定结构,S2-的核外电子排布式为:1s22s22p63s23p6,故C正确;
D.甲烷分子中含有4个碳氢共用电子对,碳原子最外层达到8电子稳定结构,甲烷的电子式为:
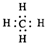 ,故D正确;
,故D正确;故选B.
点评:本题考查了比例模型、元素符号、电子式、电子排布式的判断,题目难度不大,注意掌握常见化学用语的概念及表示方法,明确离子化合物与共价化合物的概念及电子式的区别.

练习册系列答案
相关题目
分析推理是化学学习的方法之一.下列实验推理中,正确的是( )
| A、金属的冶炼方法与金属的活泼性有很大关系,所以银和汞可以用热分解的方法冶炼 |
| B、钠比铜活泼,所以钠可以从硫酸铜溶液中置换出铜 |
| C、工业上电解熔融氯化镁可制得金属镁,所以工业上电解熔融氯化铝可制得铝 |
| D、将镁条和铝片用导线连接再插进稀NaOH溶液,镁条上产生气泡,说明镁比铝活泼 |
下列有关说法中正确的是( )
| A、由氧化物组成的分子有Na2O?Al2O3?2SiO2?nH2O,可用于分离、提纯气体及作干燥剂、离子交换剂、催化剂及催化剂载体等 |
| B、大分子化合物油脂在人体内水解为氨基酸和甘油等小分子才能被吸收 |
| C、聚氯乙烯中的氯元素可以用铜丝燃烧法、钠熔法、质谱法、红外光谱法等方法进行检测 |
| D、工业上可以NaOH溶液、CS2溶液棉短绒、木浆中的纤维素,再压入酸中得到人造棉、人造丝等合成纤维 |
一定量的NaHCO3和Na2CO3混合物,向其中加入500mLHCl溶液后溶液呈中性,产生标况下CO2气体4.48L,若将等量的NaHCO3和Na2CO3混合物加热后,产生气体用碱石灰吸收,碱石灰增重4.65g,则下列叙述正确的是( )
| A、加热时生成的气体在标况下3.36L |
| B、NaHCO3和Na2CO3混合物质量为17.9g |
| C、加热时若用浓硫酸吸收气体则浓硫酸增重3.3g |
| D、HCl溶液的浓度为0.6mol/L |
Cu、Cu2O和CuO组成的混合物,加入100mL 0.6mol/LHNO3溶液恰好使混合物溶解,同时收集到224mLNO气体(标准状况).下列说法不正确的是( )
| A、产物中硝酸铜的物质的量为0.025 mol |
| B、若混合物中Cu的物质的量为x,则其中Cu2O、CuO的物质的量共0.020 mol |
| C、若混合物中含0.01moLCu,则其中Cu2O、CuO的物质的量均为0.005 mol |
| D、混合物中Cu的物质的量的取值范围为0.005mol<n(Cu)<0.015mol |
下列有机物中属于烷烃的是( )
| A、C6H12(环己烷) |
| B、C8H18(汽油的主要成分) |
| C、C8H8(立方烷) |
| D、CHBrClCF3(一种麻醉剂) |
依据下列方程式得出的结论不正确的是( )
| A、C(石墨,s)═C(金钢石,s)△H>0,说明石墨比金刚石稳定 | ||
B、NH3+H3O+?N
| ||
| C、2HCl+CaCO3═CaCl2+CO2↑+H2O,说明盐酸是强酸 | ||
| D、CH3COO-+H2O?CH3COOH+OH-,说明CH3COOH是弱电解质 |
下列各项中离子方程式的书写与反应物的用量无关的是( )
| A、FeBr2溶液与Cl2 |
| B、Ba(OH)2溶液与H2SO4溶液 |
| C、盐酸与Na2CO3溶液 |
| D、Ca(HCO3)2溶液与NaOH溶液 |
下列表示对应化学反应的离子方程式正确的是( )
| A、往FeI2溶液中通人过量氯气:Cl2+2Fe2+=2Cl-+2Fe3+ |
| B、向Na[Al(OH)4]溶液中通入少量C02:2[Al(OH)4]-+CO2=2Al(OH)3↓+C032-+H2O |
| C、向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |
| D、在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:3ClO-+Fe(OH)3=FeO42-+3Cl-+H2O+4H+ |