题目内容
块状大理石与过量的3mol?L-1盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是( )
①加入一定量的氯化钠固体 ②改用6mol?L-1盐酸 ③改用粉末状大理石 ④适当升高温度.
①加入一定量的氯化钠固体 ②改用6mol?L-1盐酸 ③改用粉末状大理石 ④适当升高温度.
分析:反应为CaCO3+2H+=Ca2++CO2↑+H2O,影响化学反应速率的因素有温度、浓度、压强、催化剂、x射线、固体物质的表面积等.增加反应物浓度,使反应速率加快;升高温度,使反应速率加快;对于有气体参与的化学反应,增大压强,使反应速率加快;增大接触面积,反应速率加快;使用正催化剂,使反应物速率加快,据此解答.
解答:解:反应为CaCO3+2H+=Ca2++CO2↑+H2O,
①加入一定量的氯化钠固体,不影响氢离子浓度,对反应速率基本无影响,故①错误;
②改用6摩/升盐酸,氢离子浓度增大,反应速率加快,故②正确;
③改用粉末状大理石 固体大理石的表面积增大,反应速率加快,故③正确;
④升高温度,反应物分子获得能量,使一部分原来能量较低分子变成活化分子,增加了活化分子的百分数,使得有效碰撞次数增多,故反应速率加大,故④正确;
故选B.
①加入一定量的氯化钠固体,不影响氢离子浓度,对反应速率基本无影响,故①错误;
②改用6摩/升盐酸,氢离子浓度增大,反应速率加快,故②正确;
③改用粉末状大理石 固体大理石的表面积增大,反应速率加快,故③正确;
④升高温度,反应物分子获得能量,使一部分原来能量较低分子变成活化分子,增加了活化分子的百分数,使得有效碰撞次数增多,故反应速率加大,故④正确;
故选B.
点评:本题考查影响化学反应速率的因素,比较基础,注意平时学习需理解记忆.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
 (2012?济南一模)(1)实验是化学研究的基础,下列有关说法中,正确的是
(2012?济南一模)(1)实验是化学研究的基础,下列有关说法中,正确的是 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到下图,则曲线a所对应的实验组别是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到下图,则曲线a所对应的实验组别是( )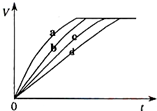 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是( )
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生气体体积V的数据,根据数据绘制得到图1,则曲线a、b、c、d所对应的实验组别可能是( )