题目内容
6.四种短周期元素A、B、C、D,A、B、C同周期,C、D同主族,E是过渡元素.A的原子结构示意图为: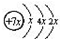 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:ASi BNa
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是HNO3.
(3)用元素符号表示D所在周期第一电离能最大的元素是Ne.
(4)D的氢化物比C的氢化物的沸点高(填“高“或“低“),原因是NH3分子间形成氢键.
(5)E元素原子的核电荷数是26,E元素在周期表的第Ⅷ族.元素周期表可按电子排布分为s区、p区等,则E元素在d区.
(6)画出D的核外电子排布图
 ,这样排布遵循了构造原理、泡利原理和洪特规则.
,这样排布遵循了构造原理、泡利原理和洪特规则.
分析 A、B、C、D是四种短周期元素,由A的原子结构示意图可知,x=2,A的原子序数为14,故A为Si元素;A、B、C同周期,B是同周期第一电离能最小的元素,故B为Na元素,C的最外层有三个成单电子,则C原子的3p能级有3个电子,故C为P元素;C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式为3d64s2,E的核外电子排布式为1s22s22p63s23p63d64s2,则E为Fe元素.
解答 解:A、B、C、D是四种短周期元素,由A的原子结构示意图可知,x=2,A的原子序数为14,故A为Si元素;A、B、C同周期,B是同周期第一电离能最小的元素,故B为Na元素,C的最外层有三个成单电子,则C原子的3p能级有3个电子,故C为P元素;C、D同主族,故D为N元素;E是过渡元素,E的外围电子排布式为3d64s2,E的核外电子排布式为1s22s22p63s23p63d64s2,则E为Fe元素.
(1)由上述分析可知,A为Si,B为Na元素,
故答案为:Si;Na;
(2)元素的非金属性越强,则最高价氧化物对应水化物酸性越强,则酸性最强的是HNO3,
故答案为:HNO3;
(3)D所在周期为第二周期,同周期中稀有气体原子为稳定结构,第一电离能最大,故第一电离能最大的元素是Ne,
故答案为:Ne;
(4)D的氢化物为NH3,C的氢化物为PH3,因为氨气分子间能形成氢键,使氨气的沸点升高,沸点高于PH3的,
故答案为:高;NH3分子间形成氢键;
(4)E为Fe元素,原子序数为26,位于周期表第四周期Ⅷ族,位于d区,
故答案为:26;Ⅷ;d;
(5)B、C最高价氧化物分别为Na2O、P2O5晶体类型分别是离子晶体、分子晶体,故答案为:离子;分子;
(6)D是N元素,原子核外有7个电子,1s、2s、2p能级上分别排列2、2、3个电子,所以其核外电子排布图为: ,这样排布遵循了构造原理、泡利原理、洪特规则,
,这样排布遵循了构造原理、泡利原理、洪特规则,
故答案为: ;泡利;洪特.
;泡利;洪特.
点评 本题考查元素推断、元素周期律、核外电子排布规律、氢键等,推断元素是解题的关键,熟练掌握元素周期律,注意同周期主族元素中第一电离能异常情况.

 阅读快车系列答案
阅读快车系列答案| A. | △H>0、△S<0 | B. | △H<0、△S>0 | C. | △H>0、△S>0 | D. | △H<0、△S<0 |
| A. | 煤的干馏,石油的裂化和裂解均属于化学变化 | |
| B. | 利用铝热反应可以冶炼Fe、Cr、Mn、W、Na等金属 | |
| C. | 甲烷和氯气制备一氯甲烷的原子利用率可达100% | |
| D. | SO2、NO2、CO2均是导致酸雨的主要原因 |
| A. | pH<7.0的降水通常称为酸雨 | |
| B. | 燃煤时加入适量石灰石,可减少废气中SO2的量 | |
| C. | 新制氯水经光照一段时间pH增大 | |
| D. | 测定氯水的pH应用干燥的pH试纸,不能用蒸馏水润湿 |
| A. | 原子半径:Al<Mg<F | B. | 热稳定性:HI>HBr>HCl>HF | ||
| C. | 酸性:H2SiO3<H3PO4<H2SO4<HClO4 | D. | 碱性:Al(OH)3>Mg(OH)2>NaOH |
| … | E | A | B | ||
| C | … | D |
(2)A与B可组成质量比为7:16的三原子分子,该分子与水反应的化学方程式:3NO2+H2O=2HNO3+NO;
(3)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若a=b,则所得溶液的pH<7(填“>“或“<”或“=”),若所得溶液的pH=7,则a>b(填“>“或“<”或“=”)
(4)写出F的单质与NaOH溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(5)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如图1所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式CO2(g)+C(s)=2CO(g)△H=+172.5kJ/mol.
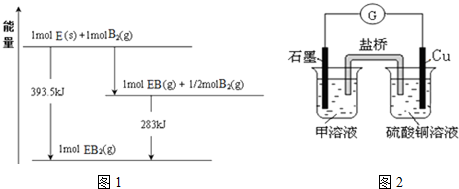
(6)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如图2所示,其反应中正极反应式为Fe3++e-=Fe2+.
| A. | CO2是氧化产物 | |
| B. | KClO3在反应中发生还原反应 | |
| C. | 生成5.6LCO2,转移的电子数目为0.25NA | |
| D. | 24.5g KClO3参加反应,转移电子物质的量为0.2mol |
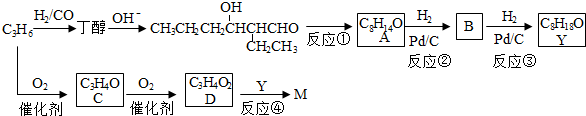
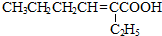 所需试剂为银氨溶液,酸.
所需试剂为银氨溶液,酸.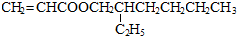
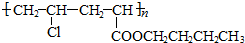
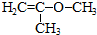 等
等