题目内容
下列条件下,可能大量共存的离子组是( )
| A、常温下水电离的c(OH-)为1×10-10 mol/L的溶液中:AlO2-、CO32-、K+、Na+ |
| B、常温下溶液中的c( H+)为1×10-5 mol/L的溶液中:S2-、SO42-、S2O32-、K+ |
| C、在含有Fe3+、Cl-的溶液中:HCO3-、I-、NH4+、Mg2+ |
| D、在含有KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl-、Br- |
考点:离子共存问题
专题:离子反应专题
分析:A.常温下水电离的c(OH-)为1×10-10 mol/L的溶液,为酸或碱溶液;
B.常温下溶液中的c( H+)为1×10-5 mol/L的溶液,显酸性;
C.离子之间相互促进水解,离子之间发生氧化还原反应;
D.离子之间发生氧化还原反应.
B.常温下溶液中的c( H+)为1×10-5 mol/L的溶液,显酸性;
C.离子之间相互促进水解,离子之间发生氧化还原反应;
D.离子之间发生氧化还原反应.
解答:
解:A.常温下水电离的c(OH-)为1×10-10 mol/L的溶液,为酸或碱溶液,碱溶液中该组离子之间不反应,可大量共存,故A选;
B.常温下溶液中的c( H+)为1×10-5 mol/L的溶液,显酸性,S2-、S2O32-、H+发生氧化还原反应,不能大量共存,故B不选;
C.Fe3+、HCO3-离子之间相互促进水解,Fe3+、I-离子之间发生氧化还原反应,不能大量共存,故C不选;
D.Fe2+、H+、NO3-离子之间发生氧化还原反应,不能大量共存,故D不选;
故选A.
B.常温下溶液中的c( H+)为1×10-5 mol/L的溶液,显酸性,S2-、S2O32-、H+发生氧化还原反应,不能大量共存,故B不选;
C.Fe3+、HCO3-离子之间相互促进水解,Fe3+、I-离子之间发生氧化还原反应,不能大量共存,故C不选;
D.Fe2+、H+、NO3-离子之间发生氧化还原反应,不能大量共存,故D不选;
故选A.
点评:本题考查离子的共存,为高频考点,把握常见离子之间的反应及习题中的信息为解答的关键,侧重氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
相关题目
 盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )
盆烯是近年合成的一种有机物,它的分子结构可简化表示为(其中C、H原子已略去),下列关于盆烯的说法中错误的是( )| A、盆烯是乙烯的一种同系物 |
| B、盆烯分子中所有的碳原子不可能在同一平面上 |
| C、盆烯是苯的一种同分异构体 |
| D、盆烯在一定条件下可以发生加成反应 |
下列说法正确的是( )
| A、纸上层析属于色谱分析法,其原理跟“毛细现象”相关,通常以滤纸作为惰性支持物,水作为固定相 |
| B、重结晶时,溶液冷却速度越慢得到的晶体颗粒越小 |
| C、用新制的Cu(OH)2浊液可以检验牙膏中的甘油,生成绛蓝色沉淀 |
| D、将3~4根火柴头浸于水中,片刻后取少量溶液于试管中,加AgNO3溶液和稀HNO3,可以检验火柴头中的氯元素 |
某同学在实验室中进行如下实验::
以下结论正确的是( )
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 | 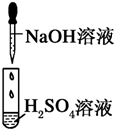 |
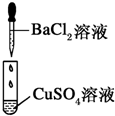 |
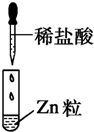 |
| 现象 | 没有明显变化,溶液仍为无色 | 有白色沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A、Ⅰ中无明显变化,说明两溶液不反应 |
| B、Ⅱ中的白色沉淀为CuCl2 |
| C、Ⅲ中的离子方程式为2H++Zn═Zn2++H2↑ |
| D、Ⅲ中发生的反应不是离子反应 |
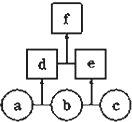 如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )
如图所示,a、b、c均为非金属单质,d、e均为含有10个电子的共价化合物,且分子中所含原子个数:d>e,f为离子化合物.则下列说法错误的是( )| A、常温下,单质a呈气态 |
| B、单质c具有强氧化性 |
| C、稳定性:d>e |
| D、f受热易分解为d和e |
下列反应属于氧化还原反应的是( )
| A、石灰石在高温下的分解反应 |
| B、生石灰和水的反应 |
| C、盐酸与氢氧化钠溶液的反应 |
| D、木炭在氧气中燃烧 |
用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是( )
| A、CuCl2[CuSO4] |
| B、NaOH[NaOH] |
| C、NaCl[HCl] |
| D、CuSO4[Cu(OH)2] |
已知 25℃时有关弱酸的电离平衡常数:
下列有关说法正确的是( )
| 弱酸化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
| A、NaHCO3溶液中,一定有c(Na+)=c(HCO3-)+c(CO32-) |
| B、1 mol?L-1HCN溶液与1mol?L-1NaOH溶液等体积混合后,测得所得溶液显酸性 |
| C、1mol/L醋酸溶液加水稀释,所有离子浓度均减小 |
| D、等物质的量浓度的各溶液pH关系为:pH(Na2CO3)>pH(NaCN)>pH(CH3COONa) |