题目内容
9.某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂.下列操作中可能使所测NaOH溶液的浓度数值偏低的是( )| A. | 酸式滴定管未用盐酸润洗就直接注入标准盐酸 | |
| B. | 滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 | |
| C. | 酸式滴定管在滴定前有气泡,滴定后气泡消失 | |
| D. | 读取盐酸体积时,开始仰视读数,滴定结束时俯视读数 |
分析 根据中和滴定不当操作对c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$中V(标准)的影响分析产生的误差,若V(标准)偏高,则测定结果偏高,若V(标准)偏低,测定结果偏低,据此进行解答.
解答 解:A.酸式滴定管未用盐酸润洗就直接注入标准盐酸,标准液被稀释,其浓度偏小,导致V(标准)偏大,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知测定较高偏高,故A错误;
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知测定结果无影响,故B错误;
C.酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知测定结果偏高,故C错误;
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$可知测定结果偏小,故D正确;
故选D.
点评 本题考查中和滴定中的误差分析,题目难度不大,明确中和滴定操作方法为解答关键,注意根据错误操作对c(待测)=$\frac{c(标准)•V(标准)}{V(待测)}$中V(标准)的影响分析误差,试题培养了学生的化学实验能力.

练习册系列答案
 学业测评一课一测系列答案
学业测评一课一测系列答案
相关题目
4.某课题组设计实验探究SO2的性质.
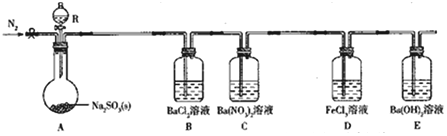
实验现象:B中无沉淀生成,C中有白色沉淀;D中溶液颜色变浅,E中产生白色沉淀.
(1)仪器R的名称是分液漏斗.
(2)实验室在常温下用80%的硫酸与亚硫酸钠粉末反应制备SO2,写出A中反应的化学方程式:Na2SO3+H2SO4═Na2SO4+SO2↑+H2O.
(3)部分实验步骤如下:连接装置、检查气密性、装药品,向装置中通入一段时间N2,然后启动A中反应.“通入一段时间的N2”的目的是排尽装置内空气,避免O2干扰实验.
(4)探究装置C中通入SO2的量与产物的关系.
①他们提出如下猜想:
猜想1:通入过量的SO2,则发生反应的离子方程式为Ba2++2NO3-+3SO2+2H2O═BaSO4↓+2SO42-+2NO+4H+.
猜想2:通入少量的SO2,则发生反应的离子方程式为3Ba2++2NO3-+3SO2+2H2O=BaSO4↓+2NO+4H+.
②请你帮他们设计实验证明猜想1和猜想2哪个合理,完成下列实验:
提供试剂:溴水、铜粉、Ba(NO3)2溶液、BaCl2溶液、Na2CO3溶液
(5)下列可检验装置D反应后溶液中是否有Fe2+的最佳试剂是c(填字母).
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.KSCN溶液和双氧水
(6)常温下,实验完毕后,分离、提纯装置E中白色固体M,取适置M于试管中,滴少量盐酸(M剩余),所得溶液的pH<7(填“>”“<”或“=”).

实验现象:B中无沉淀生成,C中有白色沉淀;D中溶液颜色变浅,E中产生白色沉淀.
(1)仪器R的名称是分液漏斗.
(2)实验室在常温下用80%的硫酸与亚硫酸钠粉末反应制备SO2,写出A中反应的化学方程式:Na2SO3+H2SO4═Na2SO4+SO2↑+H2O.
(3)部分实验步骤如下:连接装置、检查气密性、装药品,向装置中通入一段时间N2,然后启动A中反应.“通入一段时间的N2”的目的是排尽装置内空气,避免O2干扰实验.
(4)探究装置C中通入SO2的量与产物的关系.
①他们提出如下猜想:
猜想1:通入过量的SO2,则发生反应的离子方程式为Ba2++2NO3-+3SO2+2H2O═BaSO4↓+2SO42-+2NO+4H+.
猜想2:通入少量的SO2,则发生反应的离子方程式为3Ba2++2NO3-+3SO2+2H2O=BaSO4↓+2NO+4H+.
②请你帮他们设计实验证明猜想1和猜想2哪个合理,完成下列实验:
提供试剂:溴水、铜粉、Ba(NO3)2溶液、BaCl2溶液、Na2CO3溶液
| 实验步骤 | 实验现象及结论 |
| 取少量C中反应后溶液于试管中,加入铜粉(或BaCl2溶液) | 若铜粉溶解,溶液变蓝色(或无沉淀),则猜想2正确;若铜粉不溶解(或产生白色沉淀),则猜想1正确 |
a.KSCN溶液 b.NaOH溶液 c.K3[Fe(CN)6]溶液 d.KSCN溶液和双氧水
(6)常温下,实验完毕后,分离、提纯装置E中白色固体M,取适置M于试管中,滴少量盐酸(M剩余),所得溶液的pH<7(填“>”“<”或“=”).
5.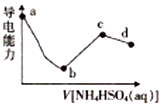 向一定浓度的Ba(OH)2溶液中滴入某浓度的NH4HSO4溶液,其导电能力随滴入溶液体积的变化如图所示.下列说法正确的是( )
向一定浓度的Ba(OH)2溶液中滴入某浓度的NH4HSO4溶液,其导电能力随滴入溶液体积的变化如图所示.下列说法正确的是( )
 向一定浓度的Ba(OH)2溶液中滴入某浓度的NH4HSO4溶液,其导电能力随滴入溶液体积的变化如图所示.下列说法正确的是( )
向一定浓度的Ba(OH)2溶液中滴入某浓度的NH4HSO4溶液,其导电能力随滴入溶液体积的变化如图所示.下列说法正确的是( )| A. | b点溶液中只存在H2O的电离平衡和BaSO4的沉淀溶解平衡 | |
| B. | c 点滚液中:c(H+)+c(NH4+)=c(NH3•H2O)+c(OH-) | |
| C. | ab段反应的离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | bc段之间存在某点,其溶液中:c(NH4+)=2c(SO42-) |
2.下列物质中溶解度最小的是( )
| A. | LiF | B. | NaF | C. | KF | D. | CsF |
4.CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g);△H=-867kJ•mol-1.该反应可用于消除氮氧化物的污染.在130℃和180℃时,分别将0.50molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如表:
(1)开展实验1和实验2的目的是研究温度对该化学平衡的影响.
(2)180℃时,反应到40min,体系是(填“是”或“否”)达到平衡状态,理由是温度升高,反应加快,对比实验1,高温下比低温下更快达到平衡状态.可确定40min时反应已经达平衡状态;CH4的平衡转化率为70%.
(3)已知130℃时该反应的化学平衡常数为6.4,试计算a的值.(写出计算过程)
(4)已知CH4(g)+4NO2(g)?4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1,求算:△H2=-1160kJ/mol.
| 实验编号 | 温度 | 0 | 10 | 20 | 40 | 50 | |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(2)180℃时,反应到40min,体系是(填“是”或“否”)达到平衡状态,理由是温度升高,反应加快,对比实验1,高温下比低温下更快达到平衡状态.可确定40min时反应已经达平衡状态;CH4的平衡转化率为70%.
(3)已知130℃时该反应的化学平衡常数为6.4,试计算a的值.(写出计算过程)
(4)已知CH4(g)+4NO2(g)?4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1,求算:△H2=-1160kJ/mol.
1.请根据所给图形回答下列问题:
(1)图表示容器中气体粒子的示意图,图中“○”和“●”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是D,可表示氯化氢(HCl)分子的是B,可表示一氧化碳和氧气的混合气体的是C(填序号).
(2)如图是水分子在一定条件下分解的示意图,从中获得的信息不正确的是C(填序号).
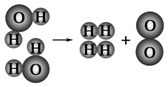
A.生成1mol O2需断开4mol H-O共价键
B.水分解后生成氢气和氧气的分子数比为2:1
C.水分解过程中,分子的种类不变
D.水分解过程中,原子的数目不变
(3)表各图中的小球代表原子序数从1~18元素的原子实(原子实是原子除最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键.下列各图表示的结构与化学式一定不相符的是C(填序号).
(1)图表示容器中气体粒子的示意图,图中“○”和“●”分别代表不同元素的原子,它们的结合体代表分子,则图中可表示氮气的是D,可表示氯化氢(HCl)分子的是B,可表示一氧化碳和氧气的混合气体的是C(填序号).
 |  | 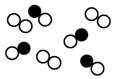 |  |
| A | B | C | D |

A.生成1mol O2需断开4mol H-O共价键
B.水分解后生成氢气和氧气的分子数比为2:1
C.水分解过程中,分子的种类不变
D.水分解过程中,原子的数目不变
(3)表各图中的小球代表原子序数从1~18元素的原子实(原子实是原子除最外层电子后剩余的部分),小黑点代表未用于形成共价键的最外层电子,短线代表共价键.下列各图表示的结构与化学式一定不相符的是C(填序号).
| A | B | C |
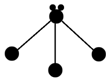 |  | 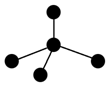 |
| NH3 | CO2 | CCl4 |
18.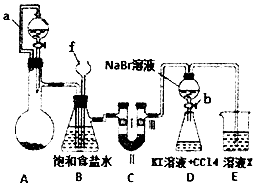 实验是化学研究的重要方法之一,某同学为了制备氯气并探究氯气等物质的相关性质,设计如图所示的实验方案:
实验是化学研究的重要方法之一,某同学为了制备氯气并探究氯气等物质的相关性质,设计如图所示的实验方案:
(1)仪器f的名称长颈漏斗.
(2)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr207),还原产物是CrCi3,写出A中离子方程式:Cr2O72-+l4H++6Cl-═2Cr3++3C12↑+7H2O.
(3)B装置的作用除了用来除去氯气中的氯化氢外还有作安全瓶,检测实验过程中装置是否堵塞.
(4)装置C的作用是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是③(填序号)
(5)利用D装置证明溴的非金属性比碘强的实验操作是:实验完毕,打开活塞b,使少量液体流入锥形瓶,关闭活塞b,振荡锥形瓶,现象是静罝分层,下层液体呈紫红色.(补充完整上述实验操作和现象)
(6)D装置进行实验时存在的明显不足是没有排除氯气对溴单质与KI反应的干扰.
 实验是化学研究的重要方法之一,某同学为了制备氯气并探究氯气等物质的相关性质,设计如图所示的实验方案:
实验是化学研究的重要方法之一,某同学为了制备氯气并探究氯气等物质的相关性质,设计如图所示的实验方案:(1)仪器f的名称长颈漏斗.
(2)A装置的分液漏斗里盛装浓盐酸,烧瓶里固体为重铬酸钾(K2Cr207),还原产物是CrCi3,写出A中离子方程式:Cr2O72-+l4H++6Cl-═2Cr3++3C12↑+7H2O.
(3)B装置的作用除了用来除去氯气中的氯化氢外还有作安全瓶,检测实验过程中装置是否堵塞.
(4)装置C的作用是探究有氧化性的物质是否一定有漂白性,下列最佳试剂组合是③(填序号)
| ① | ② | ③ | ④ | |
| I | 湿润的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 湿润的红纸条 |
| II | 碱石灰 | 浓硫酸 | 硅胶 | 氯化钠 |
| II! | 干燥的红纸条 | 干燥的红纸条 | 干燥的红纸条 | 干燥的红纸条 |
(6)D装置进行实验时存在的明显不足是没有排除氯气对溴单质与KI反应的干扰.
 在5-氨基四唑(
在5-氨基四唑(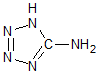 )中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.
)中加入金属Ga,得到的盐是一种新型气体发生剂,常用于汽车安全气囊.