题目内容
下列离子方程式书写正确的是( )
| A、向氧化镁中加入硫酸溶液 Mg2++SO42-═MgSO4 |
| B、向水中加入钠块 2Na+2H2O═2Na++2OH-+H2↑ |
| C、向氢氧化钡溶液中加入过量硫酸氢钠溶液 H++SO42-+Ba2++OH-═BaSO4↓+H2O |
| D、铁跟稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ |
考点:离子方程式的书写
专题:
分析:A.氧化镁为 氧化物,离子方程式中氧化镁不能拆开,硫酸镁为易溶物,离子方程式中不能保留化学式;
B.钠化学性质活泼,与水反应生成氢氧化钠和氢气;
C.硫酸氢钠过量,离子方程式按照氢氧化钡的组成书写;
D.铁与稀硫酸反应生成硫酸亚铁,不是生成铁离子.
B.钠化学性质活泼,与水反应生成氢氧化钠和氢气;
C.硫酸氢钠过量,离子方程式按照氢氧化钡的组成书写;
D.铁与稀硫酸反应生成硫酸亚铁,不是生成铁离子.
解答:
解:A.向氧化镁中加入硫酸溶液,反应生成可溶性的硫酸镁和水,正确的离子方程式为:MgO+2H+═Mg2++H2O,故A错误;
B.钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故B正确;
C.氢氧化钡溶液中加入过量硫酸氢钠溶液,离子方程式按照氢氧化钡的组成书写,正确的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D.铁与稀硫酸反应生成硫酸亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故D错误;
故选B.
B.钠与水反应生成氢氧化钠和氢气,反应的离子方程式为:2Na+2H2O═2Na++2OH-+H2↑,故B正确;
C.氢氧化钡溶液中加入过量硫酸氢钠溶液,离子方程式按照氢氧化钡的组成书写,正确的离子方程式为:2H++SO42-+Ba2++2OH-═BaSO4↓+2H2O,故C错误;
D.铁与稀硫酸反应生成硫酸亚铁,正确的离子方程式为:Fe+2H+═Fe2++H2↑,故D错误;
故选B.
点评:本题考查了离子方程式的判断,为高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
相关题目
下列各离子组可在同一溶液中大量共存,且形成无色溶液的是( )
| A、Fe2+、H+、NO3-、Cl- |
| B、Cu2+、Ba2+、Cl-、NO3- |
| C、Na+、Mg2+、OH-、SO42- |
| D、K+、Na+、OH-、NO3- |
下列反应的离子方程式书写正确的是( )
| A、钠和冷水反应:Na+2H2O=Na++2OH-+H2↑ | ||
B、金属铝溶于氢氧化钠溶液:Al+2OH-=AlO
| ||
| C、金属铝溶于盐酸中:2Al+6H+=2Al3++3H2↑ | ||
| D、AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ |
下列化学用语或模型表示正确的是( )
A、Cl-离子的结构示意图: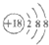 |
| B、HClO的结构式:H-O-Cl |
| C、丙烯的结构简式CH3CH2CH2 |
D、CCl4分子的球棍模型: |
下列物质的分类合理的是( )
| A、氧化物:CO2 NO SO2 H2O |
| B、碱:NaOH KOH Ba(OH)2 Na2CO3 |
| C、铵盐:NH4Cl NH4NO3 (NH4)2SO4 NH3?H2O |
| D、酸:NaHSO3 HCl H2SO4 HNO3 |
下列含有相同元素的化合物组是( )
| A、O2、O3 |
| B、CO、CO2 |
| C、KCl、AlCl3 |
| D、NaHCO3、NaHSO4 |