题目内容
设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下22.4LNH3气体中共价键总数为3NA |
| B、32g O3中含有NA个氧原子 |
| C、向装有催化剂的密闭容器加入2mol SO2和1 mol O2,充分反应后得2NA个SO3分子 |
| D、20g重水(D2O)含有10NA个中子 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.氨气分子中含有3个氮氢共价键,1mol氨气中含有3mol共价键;
B.32g臭氧中含有32g氧原子,含有2mol氧原子;
C.二氧化硫与氧气的反应为可逆反应,反应物不可能完全转化成生成物;
D.重水中含有10个中子,20g重水的物质的量为1mol,含有10mol中子.
B.32g臭氧中含有32g氧原子,含有2mol氧原子;
C.二氧化硫与氧气的反应为可逆反应,反应物不可能完全转化成生成物;
D.重水中含有10个中子,20g重水的物质的量为1mol,含有10mol中子.
解答:
解:A.标况下22.4L氨气的物质的量为1mol,1mol氨气中含有3mol氮氢共价键,含有的共价键总数为3NA,故A正确;
B.32g臭氧中含有氧原子的质量为32g,含有2mol氧原子,含有2NA个氧原子,故B错误;
C.该反应为可逆反应,2mol SO2和1 mol O2,充分反应后生成的三氧化硫的物质的量小于2mol,生成三氧化硫的分子数小于2NA,故C错误;
D.20g重水的物质的量为1mol,1mol重水中含有10mol中子,含有10NA个中子,故D正确;
故选AD.
B.32g臭氧中含有氧原子的质量为32g,含有2mol氧原子,含有2NA个氧原子,故B错误;
C.该反应为可逆反应,2mol SO2和1 mol O2,充分反应后生成的三氧化硫的物质的量小于2mol,生成三氧化硫的分子数小于2NA,故C错误;
D.20g重水的物质的量为1mol,1mol重水中含有10mol中子,含有10NA个中子,故D正确;
故选AD.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确可逆反应中,反应物的转化率不可能为100%.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
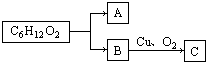 某酯的分子式为C6H12O2,其变化如图所示:若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有( )
某酯的分子式为C6H12O2,其变化如图所示:若A能发生银镜反应,C不能发生银镜反应,则该酯的可能结构有( )| A、3种 | B、4种 | C、5种 | D、6种 |
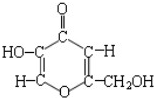 曲酸是一种非常有潜力的食品添加剂,其结构简式如图所示,试推测曲酸不可能具有的性质为( )
曲酸是一种非常有潜力的食品添加剂,其结构简式如图所示,试推测曲酸不可能具有的性质为( )| A、能发生氧化反应 |
| B、可溶于水、醇 |
| C、能发生还原反应 |
| D、分子内有三种官能团 |
下列说法中正确的是( )
| A、凡是放热反应都是自发的,由于吸热反应都是非自发的 |
| B、自发反应在恰当条件下才能实现 |
| C、催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率 |
| D、增大反应物浓度,可增大单位体积内活化分子的百分数,从而使有效碰撞次数增大 |
某微粒的核外电子排布式为1s22s22p6,下列关于该微粒的说法一定正确的是( )
| A、质子数为10 |
| B、单质具有还原性 |
| C、是单原子分子 |
| D、电子数为10 |
下列说法中,不正确的是( )
| A、化学反应中既有物质变化又有能量变化 |
| B、即使没有发生化学变化,也可能有能量的变化 |
| C、任何化学反应中的能量变化都表现为热量变化 |
| D、物质的化学能可以通过不同的变化方式转化为热能、电能等 |
下列反应属于取代反应的是( )
| A、CHCl3+HF→CHFCl2+HCl | ||
| B、CH2=CH2+H2O→CH3CH2OH | ||
| C、CH≡CH+2Br2→CHBr2-CHBr2 | ||
D、CH4
|