题目内容
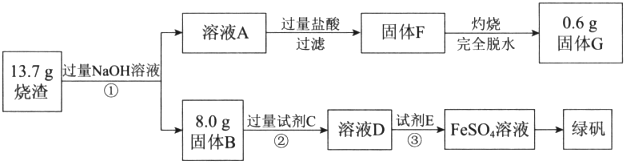
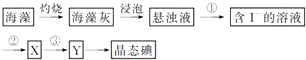
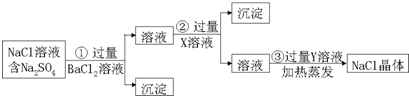
12.无水芒硝(Na2SO4)是重要的工业原料,具有十分广泛的用途.回答下列问题:Ⅰ.无水芒硝制备Na2S的流程如图(a)所示:

(1)若煅烧时,生成气体为物质的量之比1:1的CO和CO2,则发生反应的化学方程式为3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑.
(2)用稀碱液浸取比用热水好,理由为热水能促进Na2S水解,而稀碱可抑制Na2S水解.
(3)进行过滤操作时,玻璃棒的作用为引流.
(4)Na2S常用于除去皮革工业废水中的汞,汞的去除率与溶液的pH和x(x代表硫化钠的实际用量与理论用量的比值)的关系如图(b)所示.为使除汞效果最佳,应控制的条件x=12;pH的范围为9~10之间.
(5)25℃时,Ksp(HgS)=1.6×10-52.该温度下,0.1mol•L-1的Na2S溶液中,HgS的溶解度为3.728×10-50g.(假设溶液密度ρ=1.0g•mL-1)
Ⅱ.无水芒硝制备Na2S2O3.
(6)第一步:一定条件下,将H2S通入芒硝溶液中,生成Na2SO3和S;第二步:Na2SO3和S粉反应生成Na2S2O3;第三步:分离提纯.
①第一步反应的离子方程式为2H2S+SO42-+4H+═3S↓+4H2O.
②用第三步所得Na2S2O3配制成0.01000mol•L-1标准液,滴定25.00mL碘水.滴定时,所用指示剂的名称为淀粉;若滴定时平均消耗标准液的体积为10.00mL,发生的反应为2S2O32-+I2═S4O62-+2I-,则该碘水中I2的含量为5.08×10-4g•mL-1.
分析 根据图1可知,制备硫化钠晶体的流程为:无水芒硝(Na2SO4)与碳在高温煅烧反应:3Na2SO4+8C$\frac{\underline{\;高温\;}}{\;}$3Na2S+4CO2↑+4CO↑,由于硫离子水解,则用稀碱溶液浸泡抑制硫离子水解,通过精制获得硫化钠晶体,
(1)煅烧中得到等物质的量的CO和CO2,S元素被还原得到Na2S;
(2)热水促进硫化钠水解,用碱液抑制硫化钠水解;
(3)过滤操作时,玻璃棒的作用为引流;
(4)硫化钠实际用量与理论用量比值x越小、汞除去率越高,最佳效果;
(5)据Ksp(HgS)=1.6×10-52,c(S2-)=1×10-5mol/L计算可求得c(Hg2+),进而确定HgS的溶解度;
(6)①H2S通入Na2SO4溶液中,生成Na2SO3和S,根据元素守恒书写离子方程式;
②根据碘与淀粉显蓝色,选择指示剂,根据Na2S2O3的物质的量,结合2S2O32-+I2═S4O62-+2I-,计算碘的物质的量,碘水中I2的含量.
解答 解:(1)煅烧中得到等物质的量的CO和CO2,S元素被还原得到Na2S,反应方程式为:3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑;
故答案为:3Na2SO4+8C$\frac{\underline{\;\;△\;\;}}{\;}$3Na2S+4CO2↑+4CO↑;
(2)Na2S是强碱弱酸盐,水解后溶液显碱性,加热会促进S2-水解,而加碱则可以抑制其水解,
故答案为:热水能促进Na2S水解,而稀碱可抑制Na2S水解;
(3)进行过滤操作时,玻璃棒的作用为引流;
故答案为:玻璃棒的作用为引流;
(4)硫化钠实际用量与理论用量比值x越小、汞除去率越高,最佳效果,由图象可知当pH介于9~10时,x=12时汞的除去率最大,
故答案为:12;9~10之间;
(5)据Ksp(HgS)=1.6×10-52,c(S2-)=0.1mol/L计算可求得c(Hg2+)=1.6×10-51mol/L,所以HgS溶解度为1.6×10-51×(32+201)×$\frac{100}{1000}$g=3.728×10-50g,
故答案为:3.728×10-50g;
(6)①H2S通入Na2SO4溶液中,生成Na2SO3和S,反应的离子方程式为2H2S+SO42-+4H+═3S↓+4H2O,
故答案为:2H2S+SO42-+4H+═3S↓+4H2O;
②根据碘与淀粉显蓝色,所以选择淀粉作指示剂,根据题意,Na2S2O3的物质的量为0.01000mol•L-1×10.00mL=1.0×10-4 mol,结合2S2O32-+I2═S4O62-+2I-,可知碘的物质的量为5.0×10-5 mol,所以碘水中I2的含量为$\frac{5.0×10{\;}^{-5}mol×254g/mol}{0.025L}$=5.08×10-4 g•mL-1,
故答案为:淀粉;5.08×10-4.
点评 本题考查了物质制备、电解原理及其应用等知识,题目难度中等,试题涉及物质制备原理、化学方程式书写方法、电解原理及电极反应式的书写、溶度积常数的计算等,试题侧重考查学生的分析、理解能力及灵活应用所学知识的能力,是一道质量较好的题目.

 习题精选系列答案
习题精选系列答案| A. | 稀硝酸滴在大理石上:CaCO3+2H+=Ca2++H2CO3 | |
| B. | 硫酸与氢氧化钡反应:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| C. | 氧化铜与稀硫酸反应:2H++O2-═H2O | |
| D. | 碳酸钠溶液中加入盐酸:CO32-+2H+═CO2↑+H2O |
 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O
+H2O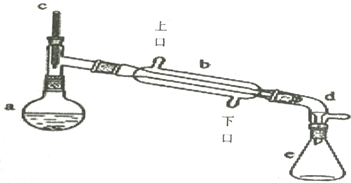
可能用到的有关数据如下:
| 相对分子质量 | 密度/(g.cm-3) | 沸点/℃ | 溶解性 | |
| 环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃氯化钙.最终通过蒸馏得到纯净环己烯10g.
回答下列问题:
(1)装置b的名称是冷凝管
(2)加入碎瓷片的作用是防暴沸.
(3)在本实验分离过程中,产物应该从分液漏斗的A
A.上口倒出 B.下口放出
(4)在本实验合成反应过程中,b中如何通入冷却水B
A.上口流进下口流出 B.下口流进上口流出
(5)在环己烯粗产物蒸馏过程中,不可能用到的仪器有C(填正确答案标号).
A.圆底烧瓶 B.温度计 C.蒸发皿 D.酒精灯 E.接收器
(6)分离提纯过程中加入无水氧化钙的目是除水
(7)本实验中最容易产生的副产物的结构简式为

(8)本实验所得到的环己烯产率是61%(结果化成百分数).
| A. | a=b | B. | a<b<2a | C. | 2a=b | D. | 2a<b |
已知:

| 密度(g/cm3) | 熔点(℃) | 沸点(℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
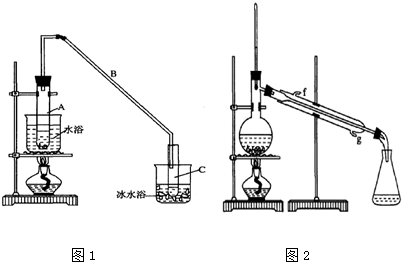
将12.5mL环己醇加入试管A中,再加入lmL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.
①水浴加热的优点是受热均匀,导管B除了导气外还具有的作用是冷凝.
②试管C置于冰水浴中的目的是进一步冷却,防止环己烯挥发.
(2)制备精品
①环己烯粗品中含有环己醇和少量酸性杂质等.加入饱和食盐水,振荡、静置、分层,环己烯在上层(填上或下),分液后用c (填入编号)洗涤.
a.KMnO4溶液 b.稀H2SO4 c.Na2CO3溶液
②再将环己烯按图2装置蒸馏,冷却水从g口进入.蒸馏时要加入生石灰,目的是除去了残留的水.
③收集产品时,控制的温度应在83℃左右,实验制得的环己烯精品质量低于理论产量,可能的原因是
a.蒸馏时从70℃开始收集产品b.环己醇实际用量多了
c.制备粗品时环己醇随产品一起蒸出
(3)以下区分环己烯精品和粗品的方法,合理的措施是bc.
a.用酸性高锰酸钾溶液 b用金属钠 c测沸点.
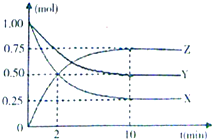 某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.
某温度时,在一个容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.