题目内容
体积为1L的某溶液中含有的离子如表所示:用Pt电极电解该溶液,当电路中有3mol电子通过时(忽略电解时溶液体积的变化及电解产物可能存在的溶解现象),下列说法正确的是( )
| 离子 | Cu2+ | Al3+ | NO3- | Cl- |
| 1 | 1 | a | 1 |
| A、阴极析出的金属是铜与铝 |
| B、a=3 |
| C、阳极生成1.5 mol Cl2 |
| D、电解后溶液的pH=0 |
考点:电解原理
专题:
分析:溶液中含有离子为n(Cu2+)=1mol/L,n(Al3+)=1mol/L,n(NO3-)=amol/L,n(Cl-)=1mol/L;H+、OH-;阳极电极反应为Cl-、OH-放电;阴极电极反应可以是Cu2+;H+;依据离子物质的量和电极反应电子转移守恒计算.
解答:
解:依据电解过程中存在电子守恒,结合电极反应计算分析产物,用Pt电极电解该溶液,当电路中有3mol e-通过时
阳极电极反应为:2Cl--2e-=Cl2↑;
1mol 1mol 0.5mol
4OH--4e-=2H2O+O2↑
2mol 2mol 1mol
阴极电极反应为:Cu2++2e-=Cu
1mol 2mol 1mol
2H++2e-=H2↑
1mol 1mol 0.5mol
A、阴极析出的金属是铜,无金属铝析出,故A错误;
B、依据溶液中电荷守恒计算忽略氢离子和氢氧根离子浓度:2c(Cu2+)+3c(Al3+)=c(Cl-)+c(NO3-),计算得到c(NO3-)=4mol/L,即a=4,故B错误;
C、依据电极反应、电子守恒可知阳极生成0.5molCl2,故C错误;
D、电解后溶液PH计算,依据两电极上的反应计算,阳极减少2mol氢氧根离子,同时阴极上减少1mol氢离子,综合计算分析得到溶液中增加氢离子物质的量为1mol,氢离子浓度为1mol/L,pH=0,故D正确;
故选D.
阳极电极反应为:2Cl--2e-=Cl2↑;
1mol 1mol 0.5mol
4OH--4e-=2H2O+O2↑
2mol 2mol 1mol
阴极电极反应为:Cu2++2e-=Cu
1mol 2mol 1mol
2H++2e-=H2↑
1mol 1mol 0.5mol
A、阴极析出的金属是铜,无金属铝析出,故A错误;
B、依据溶液中电荷守恒计算忽略氢离子和氢氧根离子浓度:2c(Cu2+)+3c(Al3+)=c(Cl-)+c(NO3-),计算得到c(NO3-)=4mol/L,即a=4,故B错误;
C、依据电极反应、电子守恒可知阳极生成0.5molCl2,故C错误;
D、电解后溶液PH计算,依据两电极上的反应计算,阳极减少2mol氢氧根离子,同时阴极上减少1mol氢离子,综合计算分析得到溶液中增加氢离子物质的量为1mol,氢离子浓度为1mol/L,pH=0,故D正确;
故选D.
点评:本题考查了电解原理的应用,电极产物的判断和计算,电极反应遵循电子守恒,依据离子物质的量和电极反应中的电子守恒计算分析判断,综合性较强.

练习册系列答案
相关题目
下列物质属于塑料的是( )
| A、聚乙烯 | B、锦纶 |
| C、阿胶 | D、玻璃钢 |
在0.1mol/L的Na2CO3溶液中,下列关系式不正确的是( )
| A、c(Na+)+c(H+)=c(HCO3-)+c(OH-)+2c(CO32-) |
| B、c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| C、c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D、c(HCO3-)+c(CO32-)+c(H2CO3)=0.1mol/L |
可以用于鉴别淀粉溶液和蛋白质溶液的方法是( )
| A、分别加入碘水,观察颜色反应 |
| B、分别加热,观察是否生成沉淀 |
| C、加入淀粉酶观察是否水解 |
| D、分别灼烧,闻味道 |
 ),其过程如下:
),其过程如下: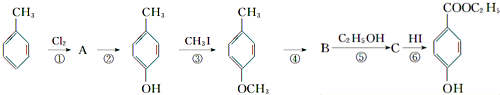
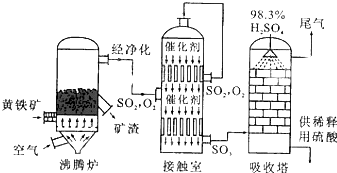 工业上常用硫磺矿或黄铁矿为原料生产硫酸,我国主要以黄铁矿为主,下面是用黄铁矿为原料生产硫酸的工艺流程图:
工业上常用硫磺矿或黄铁矿为原料生产硫酸,我国主要以黄铁矿为主,下面是用黄铁矿为原料生产硫酸的工艺流程图: