题目内容
4.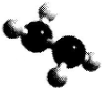 肼(N2H2)是火箭常用的高能燃料,常温下为液体,其球棍模型如图所示.肼能与双氧
肼(N2H2)是火箭常用的高能燃料,常温下为液体,其球棍模型如图所示.肼能与双氧水发生反应:NH2+2H2O2═N2+4H2O.用NA表示阿伏伽德罗常数,下列说法正确
的是( )
| A. | 标准状况下,11.2LN2中含电子总数为5 NA | |
| B. | 标准状况下,22.4LN2 H4 中所含原子总数为6 NA | |
| C. | 标准状况下,3.2gN 2H4 中含有共价键的总数为0.6 NA | |
| D. | 若生成3.6gH2 O,则上述反应转移电子的数目为0.2 NA |
分析 A.依据n=$\frac{V}{Vm}$计算氮气的物质的量,结合1个氮气分子含有14个电子解答;
B.标况下,N2 H4 为液体;
C.求出肼的物质的量,然后根据1mol肼中含5mol共价键来分析;
D.在反应中,氧元素的价态由-1价变为-2价.
解答 解:A.标准状况下,11.2LN2中含电子总数为$\frac{11.2L}{22.4L/mol}$×14×NA=7NA,故A错误;
B.标况下,N2 H4 为液体,不能使用气体摩尔体积,故B错误;
C.3.2g肼的物质的量为n=$\frac{3.2g}{32g/mol}$=0.1mol,而1mol肼中含5mol共价键,故0.1mol肼中含0.5mol共价键即0.5NA个,故C错误;
D.在反应中,氧元素的价态由-1价变为-2价,故当生成3.6g水即0.2mol水时,转移0.2mol电子即0.2NA个,故D正确;
故选:D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,注意气体摩尔体积使用条件和对象,题目难度中等.

练习册系列答案
相关题目
14.某小组利用H2O2溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.实验时,先分别量取两种溶液,然后倒入试管中迅速振荡混合均匀,开始计时,通过测定褪色所需时间来判断反应的快慢.该小组设计了如下的方案.
(1)已知反应后H2O2转化为O2逸出,KMnO4转化为MnSO4,请写出该反应的离子方程式5H2O2+2MnO4-+6H+=2Mn2++5O2↑+8H2O.
(2)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是①和②.
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=0.01 mol•L-1•min-1.
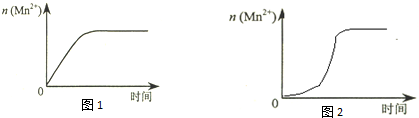
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示.
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.
①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
③若该小组同学提出的假设成立,应观察到的现象是与实验①比较,溶液褪色所需时间短(或所用时间(t)小于40s).
| 编号 | H2O2溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
(2)探究温度对化学反应速率影响的实验编号是②和③(填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是①和②.
(3)实验①测得KMnO4溶液的褪色时间为40s,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(KMnO4)=0.01 mol•L-1•min-1.
(4)该小组同学根据经验绘制了n(Mn2+) 随时间变化趋势的示意图,如图1所示.但有同学查阅已有的实验资料发现,该实验过程中n(Mn2+) 随时间变化的趋势应如图2所示.
该小组同学根据图2所示信息提出了新的假设,并继续进行实验探究.

①该小组同学提出的假设是生成物中的MnSO4为该反应的催化剂(或Mn2+对该反应有催化作用).
②请你帮助该小组同学完成实验方案,并填写表中空白.
| 编号 | H2O2溶液 | 酸性KMnO4溶液 | 温度/℃ | 再向试管中加入少量固体 | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | |||
| ④ | 0.10 | 2.0 | 0.010 | 4.0 | 25 | |
12.能正确表示下列化学反应的离子方程式是( )
| A. | 稀盐酸与铁粉反应:Fe+2H+=Fe2++H2↑ | |
| B. | 碳酸钡溶于醋酸:BaCO3+2H+=Ba2++H2O+CO2↑ | |
| C. | 锌片插入硝酸银溶液中:Zn+2Ag+=Zn2++2Ag | |
| D. | 硫酸铜溶液与氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓ |
19.常温下,下列各组离子在制定溶液中一定能大量共存的是( )
| A. | 在pH=12溶液中:Na+、Ca2+、HCO3-、ClO- | |
| B. | 在能使石蕊变红的溶液中:Mg2+、K+、Br-、SO4 2- | |
| C. | 在0.1mol•L-1的NaHCO3 溶液中:K+、Al3+、I-、Cl- | |
| D. | 在与Al 反应能放出H2 的溶液中:Fe2+、K+、NO3-、SO4 2- |
9.如图表示某高分子化合物的结构片断.关于该高分子化合物的推断正确的是( )
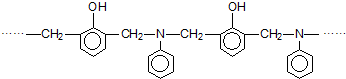

| A. | 3种单体通过加聚反应聚合 | B. | 形成该化合物的单体只有2种 | ||
| C. | 其中一种单体为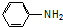 | D. | 其中一种单体为1,5-二甲基苯酚 |
16.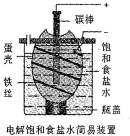 某化学课外学习小组设计电解饱和食盐水的简易装置如图(蛋壳内及壳外容器均充满饱和食盐水).有关说法正确的是( )
某化学课外学习小组设计电解饱和食盐水的简易装置如图(蛋壳内及壳外容器均充满饱和食盐水).有关说法正确的是( )
 某化学课外学习小组设计电解饱和食盐水的简易装置如图(蛋壳内及壳外容器均充满饱和食盐水).有关说法正确的是( )
某化学课外学习小组设计电解饱和食盐水的简易装置如图(蛋壳内及壳外容器均充满饱和食盐水).有关说法正确的是( )| A. | 通电一段时间后,往蛋壳内溶液中滴加几滴酚酞,呈红色 | |
| B. | 蛋壳表面缠绕的铁丝发生氧化反应 | |
| C. | 碳棒上产生的气体能使湿润的淀粉碘化钾试纸变蓝 | |
| D. | 电解一段时间后,蛋壳外溶液的pH下降 |
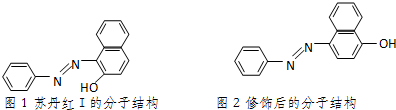
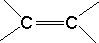 )中的π键不能自由旋转,因此CH3CH=CHCH3有两种顺反异构体.苏丹红Ⅰ号的分子结构如图1所示,分子中所有原子有(填“有”或“不”)可能在同一平面上.它的另一顺反异构体的结构简式为
)中的π键不能自由旋转,因此CH3CH=CHCH3有两种顺反异构体.苏丹红Ⅰ号的分子结构如图1所示,分子中所有原子有(填“有”或“不”)可能在同一平面上.它的另一顺反异构体的结构简式为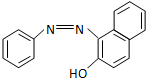 .苏丹红Ⅰ号在水中的溶解度很小,微溶于乙醇,若把羟基取代在对位形成图2所示结构,则其溶解度会增大,熔点升高(填“升高”或“降低”).下面两种物质的物理性质存在上述差异的原因可能是苏丹红I号形成分子内氢键,而修饰后的分子形成分子间氢键,分子间氢键有利于增加分子间作用力,从而有利于增大化合物的溶解度和提高熔点.
.苏丹红Ⅰ号在水中的溶解度很小,微溶于乙醇,若把羟基取代在对位形成图2所示结构,则其溶解度会增大,熔点升高(填“升高”或“降低”).下面两种物质的物理性质存在上述差异的原因可能是苏丹红I号形成分子内氢键,而修饰后的分子形成分子间氢键,分子间氢键有利于增加分子间作用力,从而有利于增大化合物的溶解度和提高熔点.