题目内容
为测定某K2SO4溶液的浓度,取25.00ml待测液,向其中加入过量的BaCl2溶液,充分反应后过滤并干燥,得到BaSO4沉淀1.165g.该K2SO4的物质的量浓度是多少?(按步骤得分)
考点:化学方程式的有关计算
专题:计算题
分析:发生反应K2SO4+BaCl2═BaSO4↓+2KCl,沉淀1.165g为硫酸钡的质量,结合n=
、c=
计算.
| m |
| M |
| n |
| V |
解答:
解:n(BaSO4)=
=0.005mol,由K2SO4+BaCl2═BaSO4↓+2KCl可知,n(K2SO4)=n(BaSO4)=0.005mol,
则该K2SO4的物质的量浓度是
=0.2mol/L,
答:该K2SO4的物质的量浓度是0.2mol/L.
| 1.165g |
| 233g/mol |
则该K2SO4的物质的量浓度是
| 0.005mol |
| 0.025L |
答:该K2SO4的物质的量浓度是0.2mol/L.
点评:本题考查化学反应方程式的计算,为高频考点,把握发生的反应及反应中物质的量的关系为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列各项比较中前者高于(或大于或强于)后者的是( )
| A、金属Mg和金属Cu的空间利用率 |
| B、C-O和Si-O的键能 |
| C、H2SO3和H2SO4中心原子的价层电子对数 |
D、邻羟基苯甲醛(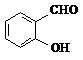 )和对羟基苯甲醛( )和对羟基苯甲醛(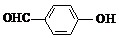 )的沸点 )的沸点 |
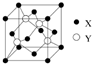 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1.元素Y基态原子的3p轨道上有5个电子.元素Z的原子最外层电子数是其内层的3倍.元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1.元素Y基态原子的3p轨道上有5个电子.元素Z的原子最外层电子数是其内层的3倍.元素W基态原子的核外电子共有16种运动状态.