题目内容
20.下列叙述正确的是( )| A. | 95℃纯水的pH<7,说明加热可导致水呈酸性 | |
| B. | pH=3的醋酸溶液,稀释至10倍后pH=4 | |
| C. | 用pH相等的盐酸、醋酸分别中和等体积等浓度的NaOH溶液,消耗两种酸的体积大小关系是:V(盐酸)>V(醋酸) | |
| D. | 室温下pH=3的醋酸溶液与pH=11的醋酸钠溶液中水电离出的C(H+)相等 |
分析 A.纯水中氢离子浓度等于氢氧根离子浓度,溶液呈中性;
B.醋酸的弱电解质,醋酸溶液中存在醋酸电离平衡;
C.pH相等的盐酸、醋酸,醋酸的浓度大于氢离子浓度,盐酸的浓度等于氢离子浓度;
D.醋酸抑制水的电离,醋酸钠促进水的电离.
解答 解:A.温度升高,水的电离程度增大,所以95℃纯水的pH<7;但是纯水中氢离子与氢氧根离子浓度相等,溶液显示中性,故A错误;
B.pH=3的醋酸溶液,溶液中氢离子浓度为0.001mol/L,稀释后醋酸的电离程度增大,溶液中氢离子的物质的量增加,当稀释至10倍后溶液中氢离子浓度大于0.0001mol/L,溶液的pH小于4,故B错误;
C.pH相等的盐酸、醋酸,醋酸的浓度大于氢离子浓度,盐酸的浓度等于氢离子浓度,所以醋酸的浓度大于盐酸的浓度,因此,消耗两种酸的体积大小关系是:V(盐酸)>V(醋酸),故C正确;
D.醋酸电离出氢离子抑制水的电离,醋酸钠水解促进水的电离,所以醋酸钠中水电离出的氢离子浓度大于醋酸溶液中水电离的氢离子浓度,故D错误;
故选C.
点评 本题考查了弱电解质在溶液中的电离平衡、盐的水解,题目难度中等,明确溶液的pH与溶液酸碱性的关系,本题旨在巩固基础,培养学生分析、理解能力.

练习册系列答案
相关题目
9.下列有关物质分类或归类正确的一组是( )
| A. | 漂白粉是化合物 | B. | 水玻璃是纯净物 | C. | 盐酸是电解质 | D. | 纯碱不属于碱 |
15.某品牌白酒中含有的塑化剂的主要成分为邻苯二甲酸二丁酯,其结构简式为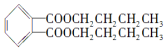 ,下列有关说法正确的是( )
,下列有关说法正确的是( )
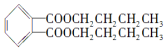 ,下列有关说法正确的是( )
,下列有关说法正确的是( )| A. | 邻苯二甲酸二丁酯的分子式为C16H21O4 | |
| B. | 用邻苯二甲酸与1-丁醇合成邻苯二甲酸二丁酯的反应属于取代反应 | |
| C. | 邻苯二甲酸二丁酯属于酯类,可增加白酒的香味,对人体无害 | |
| D. | 邻苯二甲酸二丁酯不能发生加成反应 |
5.在强酸性的无色溶液中,一定可以大量共存的离子组是( )
| A. | NH4+、Na+、CO32-、Cl- | B. | K+、Ba2+、Cl-、NO3- | ||
| C. | K+、Na+、OH-、SO42- | D. | Na+、Cu2+、Cl-、NO3- |
12.10mL浓硝酸和1.92g铜反应,铜完全溶解,生成的气体颜色由深变浅(生成NO2、NO),共收集到1.12L气体(标准状况),剩余酸用NaOH中和,共耗去1mol•L-1氢氧化钠10mL.则浓HNO3物质的量浓度为( )
| A. | 5mol•L-1 | B. | 9mol•L-1 | C. | 11mol•L-1 | D. | 12mol•L-1 |
9.向10mL浓度均为3mol•L-1的HNO3与H2SO4的混合溶液中加入1.92g铜,充分反应后,设溶液体积仍为10mL,则产生的气体在标准状况下的体积是多少升( )
| A. | 0.448 L | B. | 0.224L | C. | 0.336L | D. | 无法求解 |
10.下列事实不属于盐类水解应用的是( )
| A. | 将氯化铝溶液加热蒸干灼烧可得到氧化铝 | |
| B. | 实验室通常使用热的纯碱溶液去除油污 | |
| C. | 铵态氮肥不宜与草木灰混合使用 | |
| D. | 用大理石与醋酸制取少量二氧化碳 |
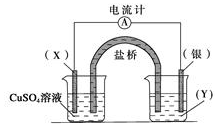 依据反应:2Ag+(aq)+Cu(s)=Cu2+ (aq)+2Ag(s)设计的原电池如图所示.
依据反应:2Ag+(aq)+Cu(s)=Cu2+ (aq)+2Ag(s)设计的原电池如图所示.