题目内容
1.(写出具体的计算过程)把5mol A和3mol B两种气体混合放入容积为2L的密闭容器里发生反应:3A(g)+B(g)?xC(g)+2D(g),经5s后反应达到平衡,在此5s内C的平均反应速率为0.4mol/(L•s),同时生成2mol D,试求(1)在此5s内D的平均反应速率.
(2)计算x的值.
(3)该反应的化学平衡常数表达式为K=$\frac{{c}^{4}(C)×{c}^{2}(D)}{{c}^{3}(A)×c(B)}$.
(4)平衡时A的转化率是多少.
分析 (1)D的浓度变化量为2mol÷2L=1mol/L,根据v=$\frac{△c}{△t}$计算v(D);
(2)利用速率之比等于化学计量数之比计算x;
(3)化学平衡常数是指:一定温度下,可逆反应到达平衡时,生成物的浓度系数次幂之积与反应物的浓度系数次幂之积的比,固体、纯液体不需要在化学平衡常数中写出;
(4)由方程式可知参加反应的n(A)=$\frac{3}{2}$n(D),再根据转化率定义计算A的转化率.
解答 解:(1)D的浓度变化量为2mol÷2L=1mol/L,则v(D)=$\frac{1mol/L}{5s}$=0.2mol/(L.s),
答:5s内D的平均反应速率为0.2mol/(L.s);
(2)速率之比等于化学计量数之比,则x:2=0.4mol/(L.s):0.2mol/(L.s),解得x=4,
答:x的值为4;
(3)3A(g)+B(g)?4C(g)+2D(g)的化学平衡常数表达式K=$\frac{{c}^{4}(C)×{c}^{2}(D)}{{c}^{3}(A)×c(B)}$,
故答案为:$\frac{{c}^{4}(C)×{c}^{2}(D)}{{c}^{3}(A)×c(B)}$;
(4)由方程式可知参加反应的n(A)=$\frac{3}{2}$n(D)=$\frac{3}{2}$×2mol=3mol,故A的转化率为$\frac{3mol}{5mol}$×100%=60%,
答:平衡时A的转化率是60%.
点评 本题考查化学反应速率有关、化学平衡计算、化学平衡常数等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
相关题目
5.在相同状况下,体积不相同的三个烧瓶中分别盛满了NH3、HCl和NO2,将它们倒扣在水槽中充分溶解后,塞住瓶口取出,烧瓶内三溶液物质的量浓度之比为( )
| A. | 1:1:1 | B. | 2:2:3 | C. | 3:3:2 | D. | 无法判断 |
9.有A、B、C、D、E五种常见化合物,都是由下表中的离子形成的:
为了鉴别上述化合物.分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其它均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入氯化钡溶液,再加过量稀盐酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验写出A、B、C的化学式:
ANaHCO3 BKNO3; CKAl(SO4)2.
| 阳离子 | K+、Na+、Al3+、Cu2+ |
| 阴离子 | OH-、HCO3-、NO3-、SO42- |
①将它们溶于水后,D为蓝色溶液,其它均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀完全溶解;
③进行焰色反应,B、C为紫色(透过蓝色钴玻璃),A、E为黄色;
④在各溶液中加入氯化钡溶液,再加过量稀盐酸,A中放出无色气体,C、D中产生白色沉淀,B中无明显现象.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验写出A、B、C的化学式:
ANaHCO3 BKNO3; CKAl(SO4)2.
16.在抗震救灾中要用大量漂白粉和漂白液杀菌消毒.下列说法正确的是( )
| A. | 漂白粉是混合物,漂粉精是纯净物 | |
| B. | 工业上将氯气通入澄清石灰水制取漂白粉 | |
| C. | 漂白粉的有效成分是Ca(ClO)2 | |
| D. | 漂白液的有效成份是Na2O2 |
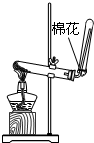
6.下列有关实验装置及用途叙述正确的是( )
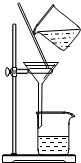
| A. |  装置用于检验消去产物 | B. | 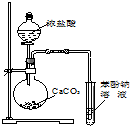 装置检验酸性:盐酸>碳酸>苯酚 | ||
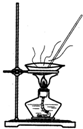
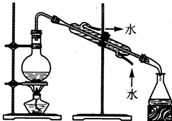
| C. | 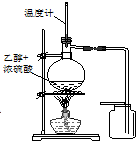 装置用于实验室制取并收集乙烯 | D. | 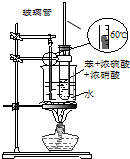 装置用于实验室制硝基苯 |
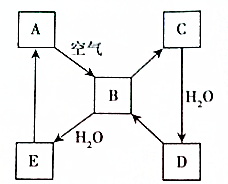 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.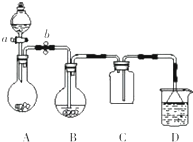 某化学小组设计了如图所示装置.用以探究Cu跟浓H2SO4的反应并收集少量气态产物(加热及夹持装置省略).
某化学小组设计了如图所示装置.用以探究Cu跟浓H2SO4的反应并收集少量气态产物(加热及夹持装置省略).