题目内容
 A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:
A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,在一定条件下有如下转化关系,请完成下列问题:(1)若常温下A为有色气体.
①若F是一种金属单质,则F为
②若C为导致温室效应的主要成分,且其固体常作致冷剂,E具有漂白性,物质F焰色反应呈黄色,则C的电子式为
(2)若物质A中一种元素原子的最外层电子数为内层电子总数的1/5,将B和D分别溶于水,所得溶液按恰当比例混合,可得一不含金属元素的盐溶液:
①B的结构式为
②请写出B转化为C的化学方程式为
③B的稳定性
考点:无机物的推断
专题:推断题
分析:A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,由转化关系可知,B、E为短周期元素组成.
(1)①若F是一种金属单质,由转化关系可知,F为变价金属,应为Fe,B与Fe反应生成高价Fe,由于A为有色气体,与水反应生成B与E,则A为二氧化氮,B为硝酸、E为NO,C为硝酸铁、D为硝酸亚铁;
②A为有色气体,与水反应生成B与E,E具有漂白性,则A为氯气、B为HCl、E为HClO,物质F焰色反应呈黄色,含有Na元素,C为导致温室效应的主要成分,且其固体常作致冷剂,结合转化关系可知,F为碳酸钠、C为二氧化碳、D为碳酸氢钠;
(2)若物质A中一种元素原子的最外层电子数为内层电子总数的
,则该元素原子有3个电子层,最外层电子数为2,则该元素为Mg,B和D分别溶于水,所得溶液按恰当比例混合,可得一不含金属元素的盐溶液,为铵盐,A中含有氮元素,则A为Mg3N2,结合转化关系,可知B为氨气、F为氧气、C为NO、D为硝酸,E为氢氧化镁.
(1)①若F是一种金属单质,由转化关系可知,F为变价金属,应为Fe,B与Fe反应生成高价Fe,由于A为有色气体,与水反应生成B与E,则A为二氧化氮,B为硝酸、E为NO,C为硝酸铁、D为硝酸亚铁;
②A为有色气体,与水反应生成B与E,E具有漂白性,则A为氯气、B为HCl、E为HClO,物质F焰色反应呈黄色,含有Na元素,C为导致温室效应的主要成分,且其固体常作致冷剂,结合转化关系可知,F为碳酸钠、C为二氧化碳、D为碳酸氢钠;
(2)若物质A中一种元素原子的最外层电子数为内层电子总数的
| 1 |
| 5 |
解答:
解:A、B、C、D、E、F为中学化学中的常见物质,且物质A由1~2种短周期元素组成,由转化关系可知,B、E为短周期元素组成.
(1)①若F是一种金属单质,由转化关系可知,F为变价金属,应为Fe,B与Fe反应生成高价Fe,由于A为有色气体,与水反应生成B与E,则A为二氧化氮,B为硝酸、E为NO,C为硝酸铁、D为硝酸亚铁,一定浓度的B和适量F反应生成C与气体E的离子方程式:Fe+4H++NO3-═Fe3++NO↑+2H2O,
故答案为:铁;Fe+4H++NO3-═Fe3++NO↑+2H2O;
②A为有色气体,与水反应生成B与E,E具有漂白性,则A为氯气、B为HCl、E为HClO,物质F焰色反应呈黄色,含有Na元素,C为导致温室效应的主要成分,且其固体常作致冷剂,结合转化关系可知,F为碳酸钠、C为二氧化碳、D为碳酸氢钠,则:则C的电子式为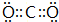 ;D的化学式为NaHCO3,
;D的化学式为NaHCO3,
故答案为: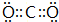 ;NaHCO3;
;NaHCO3;
(2)若物质A中一种元素原子的最外层电子数为内层电子总数的
,则该元素原子有3个电子层,最外层电子数为2,则该元素为Mg,B和D分别溶于水,所得溶液按恰当比例混合,可得一不含金属元素的盐溶液,为铵盐,A中含有氮元素,则A为Mg3N2,结合转化关系,可知B为氨气、F为氧气、C为NO、D为硝酸,E为氢氧化镁.
①B为氨气,结构式为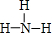 ,D为硝酸,属于共价化合物,故答案为:
,D为硝酸,属于共价化合物,故答案为: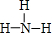 ;共价;
;共价;
②B转化为C的化学方程式为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O;
③非金属性N<O,故稳定性NH3<H2O,由OH-+NH4+═NH3+H2O,可知OH-结合质子(H+)的能力比NH3强,故答案为:<;OH-+NH4+═NH3+H2O.
(1)①若F是一种金属单质,由转化关系可知,F为变价金属,应为Fe,B与Fe反应生成高价Fe,由于A为有色气体,与水反应生成B与E,则A为二氧化氮,B为硝酸、E为NO,C为硝酸铁、D为硝酸亚铁,一定浓度的B和适量F反应生成C与气体E的离子方程式:Fe+4H++NO3-═Fe3++NO↑+2H2O,
故答案为:铁;Fe+4H++NO3-═Fe3++NO↑+2H2O;
②A为有色气体,与水反应生成B与E,E具有漂白性,则A为氯气、B为HCl、E为HClO,物质F焰色反应呈黄色,含有Na元素,C为导致温室效应的主要成分,且其固体常作致冷剂,结合转化关系可知,F为碳酸钠、C为二氧化碳、D为碳酸氢钠,则:则C的电子式为
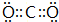 ;D的化学式为NaHCO3,
;D的化学式为NaHCO3,故答案为:
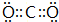 ;NaHCO3;
;NaHCO3;(2)若物质A中一种元素原子的最外层电子数为内层电子总数的
| 1 |
| 5 |
①B为氨气,结构式为
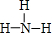 ,D为硝酸,属于共价化合物,故答案为:
,D为硝酸,属于共价化合物,故答案为: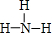 ;共价;
;共价;②B转化为C的化学方程式为:4NH3+5O2
| ||
| △ |
| ||
| △ |
③非金属性N<O,故稳定性NH3<H2O,由OH-+NH4+═NH3+H2O,可知OH-结合质子(H+)的能力比NH3强,故答案为:<;OH-+NH4+═NH3+H2O.
点评:本题考查无机物推断,熟练掌握元素化合物的性质是关键,侧重考查学生对常见物质性质与特殊反应考查,难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
现有0.4mol.L-1HA溶液和0.2mol.L-1NaOH溶液等体积混合组成的混合溶液,下列有关推断正确的是( )
| A、若HA的电离能力大于A-的水解能力,则有c(A-)>c(HA)>c(Na-)>c(OH-)>c(H-) |
| B、若该溶液中A-水解能力大于HA电离能力,则有c(A-)>c(HA)>c(Na-)>c(OH-)>c(OH+) |
| C、无论该溶液呈酸性还是碱性,都有c(Na+)=c(A-)+c(OH-) |
| D、无论该溶液呈酸性还是碱性,都有c(Na+)+c(H+)=c(A-)+c(OH-) |
分析如图装置,其中判断错误的是( )


| A、烧杯a中的溶液pH升高 |
| B、烧杯b中发生氧化反应 |
| C、盐桥中的阳离子移向烧杯a |
| D、电子从烧杯a经盐桥移向烧杯b |
常压下,150℃时,将CH4、C2H4、C3H4组成的混合气体x L与10x L氧气混合后充分燃烧,恢复到原温度和压强,则此时的气体体积为( )
| A、5x L | B、11x L |
| C、12x L | D、无法计算 |
最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的”超级温室效应气体”--全氟丙烷(C3F8),并提出用其温室化火星,使其成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
| A、分子中三个碳原子可能处在同一直线上 |
| B、它的五氯代物种数比三氯代物多 |
| C、它属于烃类 |
| D、它的分子中既有极性键又有非极性键 |
 25℃时,向20.00ml的NaOH溶液中逐滴加入某浓度的CH3COOH溶液.滴定过程中,溶液的pH与滴入CH3COOH溶液的体积的关系如图所示,②点时NaOH溶液恰好被中和.则下列说法中,错误的是( )
25℃时,向20.00ml的NaOH溶液中逐滴加入某浓度的CH3COOH溶液.滴定过程中,溶液的pH与滴入CH3COOH溶液的体积的关系如图所示,②点时NaOH溶液恰好被中和.则下列说法中,错误的是( )| A、CH3COOH溶液的浓度为0.1mol?L-1 |
| B、图中点①到点③所示溶液中,水的电离程度先增大后减小 |
| C、点④所示溶液中存在:c(CH3COOH)+c(H+)=c(CH3COO-)+c(OH-) |
| D、滴定过程中的某点,会有c(Na+)>c(CH3COO-)=c(OH-)>c(H+) |
由甲基、苯基、羟基、羧基两两结合组成的物质中,具有酸性的有多少种( )
| A、3种 | B、4种 | C、5种 | D、6种 |
下列有关叙述正确的是( )
| A、MgCO3可以转化为Mg(OH)2,则Ksp{Mg(OH)2}>Ksp(MgCO3) | ||
B、0.1ml/LNaHSO3溶液的pH为4.0,其溶液中离子浓度大小顺序为:c(Na+)>c(H+)>c(HSO
| ||
C、向pH=2的醋酸溶液中加入水稀释后,溶液中
| ||
| D、向次氯酸钙溶液中通入少量SO2反应的离子方程式为:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
