题目内容
1.常温下的下列溶液,其中酸性最弱的是( )| A. | pH=3的溶液 | B. | c(H+)=1×10-5mol/L的溶液 | ||
| C. | c(OH-)=1×10-12 mol/L的溶液 | D. | 0.005 mol/L的H2SO4溶液 |
分析 溶液中氢离子浓度越大,溶液的酸性越强,酸性最强,说明溶液中氢离子浓度最小,先将各选项的量转化成氢离子浓度,然后进行比较即可.
解答 解:A.常温下pH=3的溶液中氢离子浓度为0.001mol/L;
B.c(H+)=1×10-5mol/L的溶液;
C.c(OH-)=1×10-12 mol/L的溶液中,氢离子浓度为:$\frac{1×1{0}^{-14}}{1×1{0}^{-12}}$mol/L=0.01mol/L;
D.0.005 mol/L的H2SO4溶液中氢离子浓度为:0.005mol/L×2=0.01mol/L;
溶液中氢离子浓度越小,溶液酸性越弱,则酸性最弱的为B,
故选B.
点评 本题考查了溶液pH的简单计算,题目难度不大,明确溶液酸碱性与溶液pH的关系为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
16.除去下列物质中的杂质,根据要求填空:
| 物质 | 杂质 | 选用试剂 | 化学方程式 |
| FeCl2溶液 | FeCl3 | 铁粉 | Fe+2FeCl3=3FeCl2 |
| SiO2 | Al 2O3 | 盐酸 | Al2O3+6HCl=2AlCl3+3H2O |
| Fe(OH)3 | Al(OH)3 | NaOH溶液 | Al(OH)3+NaOH=Na[Ai(OH)4] |
10.某原电池工作时总的反应为Zn+Cu2+=Zn2++Cu,该原电池的组成可能是( )
| A. | Zn为正极,Cu为负极,CuCl2溶液作为电解质溶液 | |
| B. | Zn为负极,Cu为正极,稀H2SO4溶液作为电解质溶液 | |
| C. | Zn为负极,Cu为正极,CuSO4溶液作为电解质溶液 | |
| D. | Zn为负极,Fe为正极,Zn发生还原反应 |
11.观察煤的干馏图.下列叙述错误的是( )
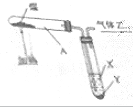

| A. | 该实验中发生了复杂的物理化学变化 | |
| B. | 液体X的pH>7 | |
| C. | Z易燃,可还原CuO | |
| D. | 试管A中产生了大量的白烟 |
