题目内容
下列关于物质的量浓度表述正确的是( )
| A、0.2 mol?L-1 Na2SO4溶液中含有Na+和SO42-总物质的量为0.6 mol |
| B、50mL 2 mol?L-1的NaCl溶液和100mL 0.5mol?L-1MgCl2溶液中,Cl-的物质的量浓度相等 |
| C、用1 L水吸收22.4 L氯化氢(标况下)所得盐酸的浓度是1 mol?L-1 |
| D、10 g 98%的硫酸(密度为1.84g?cm-3)与10mL 18.4mol?L-1的硫酸的浓度是相同的 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:A、溶液体积不知,不能计算溶液中离子数;
B、化学式中各微粒的浓度等于物质的物质的量浓度×离子个数计算;
C、溶液体积大于1L;
D、依据质量分数和物质的量浓度换算关系计算分析判断.
B、化学式中各微粒的浓度等于物质的物质的量浓度×离子个数计算;
C、溶液体积大于1L;
D、依据质量分数和物质的量浓度换算关系计算分析判断.
解答:
解:A、溶液体积不知,不能计算溶液中离子数,故A错误;
B、50mL 2 mol?L-1的NaCl溶液氯离子浓度为2mol/L,100mL 0.5mol?L-1MgCl2溶液中,Cl-的物质的量浓度0.5mol/L×2=1mol/L,所以氯离子浓度不相等,故B错误;
C、溶液体积大于1L,用1 L水吸收22.4 L氯化氢(标况下)所得盐酸的浓度小于1 mol?L-1,故C错误;
D、依据质量分数和物质的量浓度换算关系计算分析,10 g 98%的硫酸(密度为1.84g?cm-3)溶液物质的量浓度=
=18.4mol/L,与10mL 18.4mol?L-1的硫酸的浓度是相同的,故D正确;
故选D.
B、50mL 2 mol?L-1的NaCl溶液氯离子浓度为2mol/L,100mL 0.5mol?L-1MgCl2溶液中,Cl-的物质的量浓度0.5mol/L×2=1mol/L,所以氯离子浓度不相等,故B错误;
C、溶液体积大于1L,用1 L水吸收22.4 L氯化氢(标况下)所得盐酸的浓度小于1 mol?L-1,故C错误;
D、依据质量分数和物质的量浓度换算关系计算分析,10 g 98%的硫酸(密度为1.84g?cm-3)溶液物质的量浓度=
| 1000×1.84×98% |
| 98 |
故选D.
点评:本题考查了物质的量浓度概念、浓度换算,注意1L溶液吸收1mol气体,溶液体积大于1L,题目较简单.

练习册系列答案
相关题目
可用分液漏斗分离的一组混合物是( )
| A、硝基苯和酒精 |
| B、溴苯和溴 |
| C、苯和四氯化碳 |
| D、硝基苯和水 |
下列反应属于取代反应的是( )
| A、乙烯通入溴水 |
| B、苯与液溴混合后撒入铁粉 |
| C、乙醇蒸汽在铜催化作用下与氧气反应 |
| D、铁与硫酸铜溶液反应 |
下列属于电离方程式且书写正确的是( )
| A、2H2O=2H2↑+O2↑ |
| B、Ba(OH)2=Ba2++OH- |
| C、H2SO4=2H++SO42- |
| D、NaHCO3=Na++H++CO32- |
等体积的硫酸钠、硫酸镁、硫酸铝溶液分别于足量氯化钡溶液反应,若生成硫酸钡的质量相等,则三种硫酸盐的物质的量浓度之比为( )
| A、3:3:1 |
| B、6:3:2 |
| C、3:2:1 |
| D、1:1:1 |
常温时,下列关于电解质溶液的叙述正确的是( )
| A、稀释pH=10的氨水,溶液中所有离子的浓度均降低 |
| B、常温下物质的量浓度相等的①(NH4)2CO3、②NH4A1(SO4)2、③(NH4)2Fe(SO4)2三种溶液中c(NH4+):③>①>② |
| C、pH=ll的NaOH和pH=ll的氨水分别稀释100倍后的pH前者一定大于后者 |
| D、分别中和pH与体积均相同的硫酸和醋酸,硫酸消耗氢氧化钠的物质的量多 |
常温下,某无色溶液中由水电离产生的c(H+)=10-12mol/L,则此溶液中一定能大量共存的离子组是( )
| A、Mg2+、NH4+、K+、SO42- |
| B、Na+、S2O32-、OH-、Br- |
| C、Na+、K+、NO3-、SO42- |
| D、K+、Cr2O72-、NO3-、Cl- |
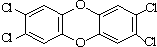 1999年比利时发生奶粉受二噁英污染事件.二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一.2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图.下列说法中不正确的是( )
1999年比利时发生奶粉受二噁英污染事件.二噁英是一类芳香族化合物的多氯代衍生物的总称,结构稳定,难以被自然分解,是公认的最危险的致癌物质之一.2,3,7,8-四氯二苯并二噁英是其中的一种,结构如图.下列说法中不正确的是( )| A、它的分子式为C12H4O2Cl4 |
| B、它的一溴取代物有一种 |
| C、它能发生取代反应 |
| D、此分子中共平面的原子最多有18个 |