题目内容
18.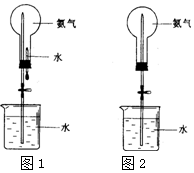 喷泉是一种常见的自然现象,其产生的原因是存在压强差.制取氨气并完成喷泉实验(图中夹持装置均已略去).
喷泉是一种常见的自然现象,其产生的原因是存在压强差.制取氨气并完成喷泉实验(图中夹持装置均已略去).(1)写出实验室制取氨气的化学方程式:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O.
(2)收集氨气应使用向下排空气法.
(3)要得到干燥的氨气可选用下列B 做干燥剂.
A.浓硫酸 B.碱石灰
(4)用图1装置进行喷泉实验,烧瓶已装满干燥氨气,引发水上喷的操作是将胶头滴管中的水挤入烧瓶中,松开弹簧夹;挤出的水溶解了烧瓶中的NH3,使瓶内压强减小,烧瓶内外形成了气压差.
(5)如果只提供如图2的装置,请说明引发喷泉措施打开止水夹,用手或热毛巾将烧瓶焐热,氨气受热膨胀赶走玻璃导管中的空气,氨气与水接触发生,即发生喷泉实验.
分析 (1)实验室用加热铵盐和碱的固体混合物制取氨气;
(2)根据氨气密度和溶解性分析解答;
(3)干燥气体时必须满足:气体不能与干燥剂反应;
(4)喷泉实验利用的原理是压强差;
(5)喷泉实验需形成明显的压力差.
解答 解:(1)实验室用加热氯化氨和消石灰的固体混合物制取氨气,方程式为2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O,
故答案为:2NH4Cl+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3+2H2O;
(2)氨气的密度比空气小,极易溶于水,只能用向下排气法收集,
故答案为:向下排空气法;
(3)浓硫酸具有酸性,氨气是碱性气体,所以,浓硫酸都不能干燥氨气,碱石灰是氢氧化钠和氧化钙的混合物呈碱性可以干燥氨气,
故答案为:B;
(4)氨气是一种极易溶于水的气体,将胶头滴管中的水挤入烧瓶中,瓶内压强减小,在外界气压的作用下,水被压到瓶内,形成喷泉现象,
故答案为:将胶头滴管中的水挤入烧瓶中,松开弹簧夹;挤出的水溶解了烧瓶中的NH3,使瓶内压强减小,烧瓶内外形成了气压差;
(5)要形成喷泉,需把烧杯中的液体压入烧瓶,可以利用吸收热量使烧瓶中的压强增大,打开止水夹,用手或热毛巾将烧瓶焐热,氨气受热膨胀赶走玻璃导管中的空气,氨气与水接触发生,即发生喷泉实验,
故答案为:打开止水夹,用手或热毛巾将烧瓶焐热,氨气受热膨胀赶走玻璃导管中的空气,氨气与水接触发生,即发生喷泉实验.
点评 本题考查了氨气的性质实验,探究了喷泉的形成,注意知识的积累,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
13.下列说法或做法正确的是( )
| A. | 正常雨水PH等于7,酸雨的PH小于7 | |
| B. | 金属钠着火燃烧时,可用泡沫灭火器灭火 | |
| C. | 在放电条件下,氮气和氧气化合生成二氧化氮 | |
| D. | 冷的浓硫酸与铁、铝反应时会使金属表面生成致密的氧化物而钝化 |
3.下列叙述不正确的是( )
| A. | 在原电池的负极和电解池的阳极上发生的都是氧化反应 | |
| B. | 实验室用惰性电极电解NaCl溶液,阴、阳两极收集到的气体体积之比为1:1 | |
| C. | 一定条件下可能发生反应:Cu+H2SO4═CuSO4+H2↑ | |
| D. | 在用惰性电极电解稀硫酸的过程中,溶液pH保持不变. |
10.某水合盐的蒸气压低于该温度下空气中水的蒸气压,这种盐会发生( )
| A. | 起泡 | B. | 风化 | C. | 潮解 | D. | 不受影响 |
7.某反应的反应物与生成物有SeO2、HNO3、KI、Se、KNO3、H2O、I2,已知氧化性:SeO2>I2,则下列说法正确的是( )
| A. | HNO3作氧化剂 | |
| B. | 氧化剂和还原剂的物质的量之比为1:1 | |
| C. | 当生成1molI2时,转移2mol电子 | |
| D. | 由该反应可知还原性:Se>KI |
1.开发新材料是现代科技发展的方向之一.下列有关材料的说法正确的是( )
| A. | 合成纤维和光导纤维都是有机高分子材料 | |
| B. | SiO2是人类将太阳能转变为电能的常用材料 | |
| C. | 水晶、玛瑙、水泥和瓷器都是硅酸盐制品 | |
| D. | 氮化硅陶瓷是新型无机非金属材料 |
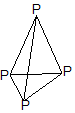 已知白磷是由P4分子形成的分子晶体,每个P4分子是正四面体结构.分子中的四个磷原子位于正四面体的四个顶点.则P4分子中共有6个P-P键.
已知白磷是由P4分子形成的分子晶体,每个P4分子是正四面体结构.分子中的四个磷原子位于正四面体的四个顶点.则P4分子中共有6个P-P键.