题目内容
乙二酸(H2C2O4)俗称草酸,是一种重要的化工原料.查阅资料,了解到以下有关信息:
①乙二酸易溶于水,加热至100℃开始升华,125℃时迅速升华,157℃时大量升华并开始分解.乙二酸受热分解生成水、二氧化碳和一种常见的还原性气体.
②乙二酸的钙盐--乙二酸钙为不溶于水的白色晶体.
(1)请写出乙二酸受热分解的化学方程式 .
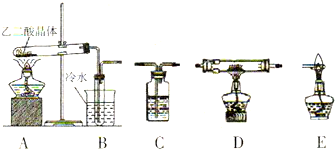
(2)化学兴趣小组的同学用实验证明乙二酸晶体受热分解生成的气体成分.他们利用如图提供的装置,自选试剂,提出了下列实验方案:按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分.请你按整套装置从左至右的顺序填写下表中的空格:
(2)上述实验中能说明乙二酸热分解生成了还原性气体的实验现象是 .
(3)检验乙二酸具有较强的还原性,通常选用的试剂是 .

①乙二酸易溶于水,加热至100℃开始升华,125℃时迅速升华,157℃时大量升华并开始分解.乙二酸受热分解生成水、二氧化碳和一种常见的还原性气体.
②乙二酸的钙盐--乙二酸钙为不溶于水的白色晶体.
(1)请写出乙二酸受热分解的化学方程式
(2)化学兴趣小组的同学用实验证明乙二酸晶体受热分解生成的气体成分.他们利用如图提供的装置,自选试剂,提出了下列实验方案:按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分.请你按整套装置从左至右的顺序填写下表中的空格:
| 装置编号 | 装置中所加物质 | 装置作用 |
| B | -------- | |
| C | ||
| C | 氢氧化钠浓溶液 | |
| C | ||
| D | ||
| E | -------- |
(3)检验乙二酸具有较强的还原性,通常选用的试剂是
考点:性质实验方案的设计
专题:实验设计题
分析:(1)根据草酸晶体受热分解生成一氧化碳、二氧化碳和水,配平反应的方程式;
(2)按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分,结合装置和试剂作用分析回答;
(2)D装置中黑色的氧化铜变红色,说明乙二酸热分解生成了还原性气体;
(3)乙二酸具有较强的还原性,能使酸性高锰酸钾溶液褪色.
(2)按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分,结合装置和试剂作用分析回答;
(2)D装置中黑色的氧化铜变红色,说明乙二酸热分解生成了还原性气体;
(3)乙二酸具有较强的还原性,能使酸性高锰酸钾溶液褪色.
解答:
解:(1)草酸晶体受热分解生成一氧化碳、二氧化碳和水,①草酸晶体受热分解生成一氧化碳、二氧化碳和水,所以反应的方程式为:H2C2O4
CO2↑+CO↑+H2O;
故答案为:H2C2O4
CO2↑+CO↑+H2O;
(2)按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分,装置B检验H2O(g);冷却凝固乙二酸蒸汽,防止其进入澄清石灰水影响CO2的检验;装置C澄清石灰水检验二氧化碳,装置C中氢氧化钠溶液吸收多余的CO2 ;装置C装有浓硫酸吸收其他中水蒸气;装置D是验证一氧化碳的生成还原金属氧化物;装置E处理剩余一氧化碳气体,防止污染气体;
故答案为:
(2)能说明乙二酸热分解生成了还原性气体CO的实验现象是 D装置中黑色的氧化铜变红色,E装置导管口气体燃烧;
故答案为:D装置中黑色的氧化铜变红色,E装置导管口气体燃烧;
(3)乙二酸具有较强的还原性,能使酸性高锰酸钾溶液褪色,故答案为:酸性高锰酸钾溶液;
| ||
故答案为:H2C2O4
| ||
(2)按A→B→C→C→C→D→E顺序从左至右连接装置,检验乙二酸晶体受热分解生成的气体成分,装置B检验H2O(g);冷却凝固乙二酸蒸汽,防止其进入澄清石灰水影响CO2的检验;装置C澄清石灰水检验二氧化碳,装置C中氢氧化钠溶液吸收多余的CO2 ;装置C装有浓硫酸吸收其他中水蒸气;装置D是验证一氧化碳的生成还原金属氧化物;装置E处理剩余一氧化碳气体,防止污染气体;
故答案为:
| 装置编号 | 装置中所加物质 | 装置作用 |
| B | ------ | 检验H2O(g);冷却凝固乙二酸蒸汽,防止其进入澄清石灰水影响CO2的检验 |
| C | 澄清石灰水 | 检验CO2 |
| C | 吸收多余的CO2 | |
| C | 浓硫酸 | 吸收水蒸气 |
| D | CuO或Fe2O3 | 检验CO |
| E | -------- | 处理CO尾气,防止污染空气 |
故答案为:D装置中黑色的氧化铜变红色,E装置导管口气体燃烧;
(3)乙二酸具有较强的还原性,能使酸性高锰酸钾溶液褪色,故答案为:酸性高锰酸钾溶液;
点评:本题属于信息题的考查,注意考查了物质的性质、检验、除杂等,综合性较强,但难度中等,关键是通过阅读众多的信息量提取有用的信息结合已有的相关知识进行解析即可.

练习册系列答案
相关题目
下列物质的水溶液能导电,但属于非电解质的是( )
| A、Na2O |
| B、Cl2 |
| C、NH4HCO3 |
| D、CO2 |
工业生产中物质的循环利用有多种模式.例如:

表述不正确的是( )

表述不正确的是( )
| A、若图I为合成氨,则其中N2、H2可循环使用 |
| B、若图I为合成SO3,则其中SO2、O2可循环使用 |
| C、若图Ⅱ为电解熔融MgCl2得到镁,则其中HCl可循环使用 |
| D、若图Ⅲ为氨氧化法制硝酸,则其中NO2可循环使用 |
有A、B两种原子,A原子的第三电子层比B原子的第三电子层少3个电子,B原子的第二电子层电子数恰好为A原子第二电子层电子数的2倍.A和B分别是( )
| A、硅原子和钠原子 |
| B、硼原子和氦原子 |
| C、氯原子和碳原子 |
| D、碳原子和铝原子 |
标准状况下22.4LH2 和C2H4的混合气体在一定条件下反应,所得气态物质完全燃烧恢复至常温后放出736KJ热量,混合气体中H2和C2H4的物质的量之比应为[已知H2、C2H4、C2H6的燃烧热(单位:KJ/mol)分别是286、1411和1560]( )
| A、1:3 | B、2:3 |
| C、3:1 | D、3:2 |
在某容器中,C+H2O(g)?CO+H2反应达到平衡,在温度、体积不变的情况下,向容器中充入一定量H2,当建立新平衡时( )
| A、CO、H2的浓度都比原平衡时的要小 |
| B、CO、H2的浓度都比原平衡时的要大 |
| C、H2、H2O(g)的浓度都比原平衡时的要大 |
| D、CO、H2O(g)的浓度都比原平衡时的要大 |
 如图是研究铜与浓硫酸的反应装置:
如图是研究铜与浓硫酸的反应装置: 某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如下图.材料1:NH3是强还原剂,能将某些金属氧化物还原为金属单质或低价态的氧化物.如:2NH3+3CuO
某研究性学习小组利用以下材料来探究NH3的还原性,部分实验装置如下图.材料1:NH3是强还原剂,能将某些金属氧化物还原为金属单质或低价态的氧化物.如:2NH3+3CuO