题目内容
2.H2A在水中存在以下平衡:H2A?H++HA-,HA-?H++A2-.(1)NaHA溶液显酸性,则溶液中离子浓度的大小顺序为c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH- ).
(2)常温时,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性.此时该混合溶液的下列关系中,一定正确的是AB.
A.c(Na+ )>c(K+ ) B.c(H +)•c(OH )=1×10-14
C.c(Na+ )=c(K+ ) D.c(Na+ )+c(K+ )=c(HA- )+c(A2-)
分析 (1)H2A是二元弱酸,其发生两步电离,且第一步电离程度远远大于第二步电离,NaHA溶液显酸性,说明HA-电离程度大于水解程度,钠离子不水解,再结合电荷守恒分析解答;
(2)常温时,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性,溶液中溶质为Na2A、NaHA,则c(H+)=c(OH );NaHA溶液呈碱性,要使混合溶液呈中性,n(NaHA)>n(KOH),再结合电荷守恒、物料守恒分析解答.
解答 解:(1)H2A是二元弱酸,其发生两步电离,且第一步电离程度远远大于第二步电离,NaHA溶液显酸性,说明HA-电离程度大于水解程度,且其程度都较小,钠离子不水解,HA-和水电离都生成氢离子,只有HA-电离生成A2-,所以离子浓度大小顺序是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故答案为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-);
(2)常温时,若向0.1mol/L的NaHA溶液中逐滴滴加0.1mol/L KOH溶液至溶液呈中性,溶液中溶质为Na2A、NaHA,则c(H+)=c(OH );NaHA溶液呈碱性,要使混合溶液呈中性,n(NaHA)>n(KOH),
A.因为n(NaHA)>n(KOH),且钠离子、钾离子都不水解,所以存在c(Na+ )>c(K+ ),故A正确;
B.离子积常数只与温度有关,温度不变,离子积常数不变,所以常温下c(H +)•c(OH )=1×10-14,故B正确;
C.根据A知c(Na+ )>c(K+ ),故C错误;
D.溶液呈中性,则c(H+)=c(OH ),结合电荷守恒得c(Na+ )+c(K+ )=c(HA- )+2c(A2-),故D错误;
故选AB.
点评 本题考查离子浓度大小比较,明确溶液中溶质及其性质是解本题关键,注意电荷守恒和物料守恒的灵活运用,难点是(2)NaHA、KOH物质的量相对大小判断,题目难度中等.

 阅读快车系列答案
阅读快车系列答案| W | X | ||
| Y | Z |
(2)Z的原子结构示意图为
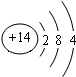
(3)X和Y离子半径最大的是N3-(填离子符号)
(4)下列选项中.能证明元素非佥属性X强于W的是CD
A.原子序数:W>X B.最低化合价:X>W
C.最简单氢化物的稳定性:X>W D.最高价氧化物的水化物酸性:X>W
(5)写出表中Y的最高价氧化物对应水化物的电离方程式Mg(OH)2?Mg2++2OH-
(6)元素周期表中与同Z同期的某金属元素形成的单质A,可发生如图所示的转化
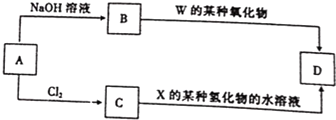
其中化含物D是-种白色沉淀,则生成物B的化学式为NaAlO2,C转化生成D的离子方程式为Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
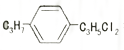 表示的有机物共有(不考虑立体结构)( )
表示的有机物共有(不考虑立体结构)( )| A. | 16种 | B. | 18种 | C. | 20种 | D. | 22种 |
| A. | NaCl | B. | NaOH | C. | NH4NO3 | D. | Ca(HCO3)2 |
 环己烯是一种重要的化工原料.
环己烯是一种重要的化工原料.(1)实验室可由环己醇制备环己烯,反应的化学方程式是
 .
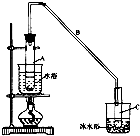
.(2)实验装置如下图所示,将10mL环己醇加入试管A中,再加入1mL浓硫酸,摇匀后放入碎瓷片,缓慢加热至反应完全,在试管C内得到环己烯粗品.环己醇和环己烯的部分物理性质如下:
| 密度 (g/cm3) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 环己醇 | 0.96 | 25 | 161 | 能溶于水 |
| 环己烯 | 0.81 | -103 | 83 | 难溶于水 |
②试管A置于水浴中的目的是受热均匀,便于控温;
试管C置于冰水浴中的目的是使环己烯液化,减少挥发.
(3)环己烯粗品中含有少量环己醇和酸性杂质.精制环己烯的方法是:
①向环己烯粗品中加入C(填入编号),充分振荡后,分液(填操作名称).
A.Br2的CCl4溶液 B.稀H2SO4 C.Na2CO3溶液
②再对初步除杂后的环己烯进行蒸馏,得到环己烯精品.蒸馏时,蒸馏烧瓶中要加入少量生石灰,目的是除去产品中少量的水.
③实验制得的环己烯精品质量低于理论产量,可能的原因是C.
A.蒸馏时从70℃开始收集产品
B.环己醇实际用量多了
C.制备粗品时环己醇随产品一起蒸出
(4)以下区分环己烯精品和粗品的方法,合理的是B.
A.加入水观察实验现象
B.加入金属钠观察实验现象
C.加入酸性高锰酸钾溶液,振荡后观察实验现象.
| A. | CO2和NaOH溶液 | B. | SO2和稀氨水 | C. | NO2和NaOH溶液 | D. | Cl2和饱和食盐水 |
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | Ba(OH)2溶液 | D. | BaCl2溶液 |
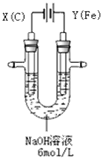 高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.
高铁酸钾(K2FeO4)具有高效的消毒作用,为一种新型非氯高效消毒剂.电解法制备高铁酸钾操作简便,成功率高,易于实验室制备.其原理如图所示.