题目内容
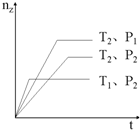 反应aX(g)+bY(g)cZ(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是( )
反应aX(g)+bY(g)cZ(g),在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量(nz)与反应时间(t)的关系如图所示.下列判断正确的是( )| A、T1<T2,P1<P2,a+b<c正反应是吸热反应 |
| B、T1<T2,P1>P2,a+b<c正反应是吸热反应 |
| C、T1>T2,P1>P2,a+b>c逆反应是吸热反应 |
| D、T1>T2,P1<P2,a+b>c逆反应是吸热反应 |
考点:化学平衡的影响因素,化学平衡建立的过程
专题:化学平衡专题
分析:根据根据先拐先平衡,条件高判断,结合升高温度,化学反应速率加快,平衡向着吸热的方向移动;增大压强,化学反应速率加快,平衡向着气体体积减小的方向移动.
解答:
解:P2时,根据先拐先平衡,温度高,则T1>T2,升高温度,Z的物质的量减小,平衡逆向移动,则正反应为放热反应;
T2时,根据先拐先平衡,压强高,P1>P2,增大压强,Z的物质的量增大,说明平衡正向移动,故a+b>c,
故选C.
T2时,根据先拐先平衡,压强高,P1>P2,增大压强,Z的物质的量增大,说明平衡正向移动,故a+b>c,
故选C.
点评:本题考查温度、压强对化学平衡的影响,难度中等.根据温度、压强与生成物Z物质的量的变化确定反应热及气体的计量数变化.

练习册系列答案
相关题目
将一小粒钠投入氯化铜溶液中,待反应停止后,观察到的现象是( )
| A、有蓝色沉淀 |
| B、有蓝色沉淀和气体产生 |
| C、有气体产生,无沉淀生成 |
| D、无沉淀和有气体产生 |
下列说法正确的是( )
| A、KClO3和SO3溶于水后能导电,故KClO3和SO3为电解质 |
| B、HClO是弱酸,所以NaClO是弱电解质 |
| C、HCl溶液和NaCl溶液均通过离子导电,所以HCl和NaCl均是离子化合物 |
| D、杂多酸盐Na2HPW12O40与Na3PW12O40都是强电解质 |
反应2SO2+O2
2SO3+Q达到化学平衡状态时的标志是( )
| 催化剂 |
| A、SO2的消耗速率等于SO3的生成速率 |
| B、SO2的生成速率等于SO3的生成速率 |
| C、SO2的消耗速率大于O2生成速率的2倍 |
| D、SO3的生成速率等于O2的生成速率 |
固体烧碱溶于水明显放热,这是因为( )
①在溶解过程中,Na+和OH-与水结合成水合离子,这是个放热过程
②Na+和OH-从烧碱固体表面向水中扩散的过程是吸热过程
③过程放热量超过了过程②的吸热量
④过程吸热量超过了过程①的放热量.
①在溶解过程中,Na+和OH-与水结合成水合离子,这是个放热过程
②Na+和OH-从烧碱固体表面向水中扩散的过程是吸热过程
③过程放热量超过了过程②的吸热量
④过程吸热量超过了过程①的放热量.
| A、①② | B、①③ |
| C、①②③ | D、①③④ |
下列有关热化学方程式的书写及对应的表述均正确的是( )
| A、密闭容器中,9.6 g硫粉与11.2 g铁粉混合加热生成17.6 g硫化亚铁时,放出19.12 kJ热量.则Fe(s)+S(s)═FeS(s)△H=-95.6 kJ?mol-1 |
| B、稀醋酸与0.1 mol?L-1 NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l)△H=-57.3 kJ?mol-1 |
| C、已知1 mol氢气完全燃烧生成液态水所放出的热量为285.5 kJ,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ?mol-1 |
| D、已知2C(s)+O2(g)=2CO(g)△H=-221 kJ?mol-1,则可知C的燃烧热△H=-110.5 kJ?mol-1 |
下列反应的离子方程式书写正确的是( )
| A、硫酸铝溶液中加入过量氨水 Al3++3OH-=Al(OH)3↓ | ||||
B、电解饱和食盐水 2Cl-+2H+
| ||||
| C、在稀氨水中通入过量CO2 NH3?H2O+CO2=NH4++HCO3- | ||||
| D、硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O |