题目内容
下列说法正确的是( )
| A、离子化合物中一定含离子键,也可能有共价键 |
| B、所有非金属之间形成的化学键一定是共价键 |
| C、电子数相同的两种微粒一定是同一元素 |
| D、共价化合物中一定无离子键 |
考点:离子化合物的结构特征与性质,共价键的形成及共价键的主要类型
专题:化学键与晶体结构
分析:A.离子化合物中一定含有离子键,可能含有共价键,共价化合物中只含共价键;
B.非金属元素之间形成的化学键可能是离子键;
C.电子数相同的两种微粒可能是不同的元素;
D.只含共价键的化合物为共价化合物.
B.非金属元素之间形成的化学键可能是离子键;
C.电子数相同的两种微粒可能是不同的元素;
D.只含共价键的化合物为共价化合物.
解答:
解:A.离子化合物中一定含有离子键,可能含有共价键,如KOH,故A正确;
B.非金属元素之间形成的化学键可能是离子键,如铵盐,故B错误;
C.电子数相同的两种微粒可能是不同的元素,如O2-、F-,故C错误;
D.只含共价键的化合物为共价化合物,共价化合物中一定不含离子键,故D正确;
故选AD.
B.非金属元素之间形成的化学键可能是离子键,如铵盐,故B错误;
C.电子数相同的两种微粒可能是不同的元素,如O2-、F-,故C错误;
D.只含共价键的化合物为共价化合物,共价化合物中一定不含离子键,故D正确;
故选AD.
点评:本题考查化合物和化学键的关系,明确物质构成微粒及微粒之间的作用力即可解答,易错选项是B.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案
相关题目
下列有关钠的物理性质的叙述中正确的是( )
①银白色金属;
②质软,可以用小刀切割;
③熔点低于100℃;
④密度比水小;
⑤热和电的良导体.
①银白色金属;
②质软,可以用小刀切割;
③熔点低于100℃;
④密度比水小;
⑤热和电的良导体.
| A、①②④ | B、①②③④ |
| C、①③④ | D、①②③④⑤ |
下列各组元素,氧化性逐渐增强的一组是( )
| A、I2、Br、Cl2、F2 |
| B、F2、Cl2、Br2、I2 |
| C、F-、Cl-、Br-、I- |
| D、Li、Na、K、Rb |
下列叙述中不正确的是( )
| A、HClO4的酸性比H2SO4强 |
| B、硫化氢的稳定性比氯化氢的强 |
| C、钠与硫化合时生成硫化钠 |
| D、氯气的氧化性比单质硫的强 |
下列有关说法正确的是( )
| A、物质熔、沸点的高低顺序是:晶体硅>氯化钠>冰>氖气 |
| B、微粒半径由大到小的顺序是:H+>Li+>H- |
| C、金刚石的硬度、熔点、沸点都低于晶体硅 |
| D、CO2、HCl、CF4、PCl3四种物质分子中的所有原子都满足最外层为8电子的稳定结构 |
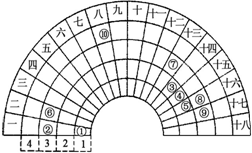 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A、②、⑧、⑨对应简单离子半径依次减小 |
| B、⑥的氯化物的熔点比⑦的氯化物熔点低 |
| C、元素⑩处于常见周期表第四周期第VIIIB族 |
| D、①、③、④、⑤形成的某种化合物中既含有共价键又含有离子键 |
 江西某铜业公司在火法炼铜时也生产硫酸,硫酸车间如图.下列叙述不正确的是( )
江西某铜业公司在火法炼铜时也生产硫酸,硫酸车间如图.下列叙述不正确的是( )| A、自然界化合态硫以FeS、CuFeS2等形式存在 |
| B、火法炼铜的矿石原料主要含Cu2S |
| C、该公司炼铜产生的SO2可用于生产H2SO4 |
| D、l mol/L H2SO4溶液可储存于铁制或铝制容器 |
某化工厂按如下步骤进行生产:①以煤为燃料煅烧石灰石;②用饱和碳酸钠溶液充分吸收步骤①中产生的二氧化碳;③使步骤①产生的氧化钙跟水反应,④熟石灰与碳酸钠溶液反应.该厂生产过程中涉及的物质有:①石灰石;②纯碱(Na2CO3);③小苏打(NaHCO3);④烧碱;⑤二氧化碳;⑥消石灰;下列叙述正确的是( )
| A、起始原料是①② |
| B、起始原料是②⑥ |
| C、最终产品是④⑤ |
| D、最终产品是③④ |
下列说法有错误的是( )
| A、可以用灼烧线头的方法鉴别纺织物是毛织物还是棉织物 |
| B、除去SO3中混有的少量SO2,可将混合气体通过盛有热浓硫酸的洗气瓶 |
| C、室温下向苯和少量苯酚的混合液中加入适量Na2CO3溶液,振荡、静置后分液,可除去苯中少量苯酚 |
| D、已知I3-?I2+I-,向盛有KI3溶液的试管中加入适量CCl4,振荡静置后CCl4层显紫色,不能说明KI3在CCl4中的溶解度比在水中的大 |