题目内容
氮的固定是指将氮元素由游离态转化为化合态的过程.
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
(1)反应需要在闪电或极高温条件下发生,说明该反应 .(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)?2NO(g)的平衡常数K如下表:
该反应的△H 0.(填“>”、“=”或“<”)
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO.
(1)反应需要在闪电或极高温条件下发生,说明该反应
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)?2NO(g)的平衡常数K如下表:
| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:(1)自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO,说明该反应难以进行,反应的活化能高;
(2)根据图表中的平衡常数随温度变化趋势是,温度越高,K值越大;依据平衡影响因素判断平衡移动.
(2)根据图表中的平衡常数随温度变化趋势是,温度越高,K值越大;依据平衡影响因素判断平衡移动.
解答:
解:(1)闪电或者高温,主要是提供能量 给N2分子,让其破坏变成氮原子,因此,只能说明 引发反应所需要的能量高即活化能,不能说明反应吸收的能量高;故答案为:A;
(2)在不同温度下,反应N2(g)+O2(g)?2NO(g)的平衡常数K随温度升高K值增大,所以正反应方向是吸热反应,△H>0,故答案为:>.
(2)在不同温度下,反应N2(g)+O2(g)?2NO(g)的平衡常数K随温度升高K值增大,所以正反应方向是吸热反应,△H>0,故答案为:>.
点评:本题考查了化学平衡常数的含义,应用条件判断,关键是平衡常数的概念应用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质长期露置在空气中不易变质的是( )
| A、漂白粉 | B、苯酚 |
| C、水玻璃 | D、碳酸钠粉末 |
下列说法错误的是;( )
| A、过量铁与浓硫酸加热反应可以得到氢气 |
| B、硅酸盐NaAlSiO4?nH2O可改写成氧化物形式为:Na2O?Al2O3?2SiO2?2nH2O |
| C、某雨水样品采集后放置一段时间,pH由4.68变为4.28,是因为水中溶解了较多的CO2 |
| D、Al65Cu23Fe12是一种拟晶,具有合金的优良物理性能,其硬度比金属A1、Cu、Fe都大 |
将铜粉放入稀硫酸中,加热无明显反应发生.但加入某盐后,发现铜粉质量逐渐减少,该盐是( )
| A、FeSO4 |
| B、ZnSO4 |
| C、KNO3 |
| D、NaCl |
下列生产工艺措施合理的是( )
| A、用SO2漂白银耳 |
| B、用硫酸清洗锅炉中的水垢 |
| C、高温下用镁还原SiO2制取粗硅 |
| D、用Na2S作沉淀剂,除去废水中Cu2+和Hg2+ |
三氟化氮(NF3)是一种新型电子材料,它在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3.下列有关说法正确的是( )
| A、反应中NF3是氧化剂,H2O是还原剂 |
| B、反应中被氧化与被还原的原子物质的量之比为2:1 |
| C、若反应中生成0.2 mol HNO3,则反应共转移0.2 mol e- |
| D、NF3在潮湿空气中泄漏会产生白雾、红棕色气体等现象 |
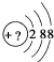 (1)该微粒是中性微粒,这种微粒的符号是
(1)该微粒是中性微粒,这种微粒的符号是