题目内容
17.用NA表示阿伏伽德罗常数,下列叙述中正确的是( )| A. | 12g 12C含中子数为NA | |
| B. | 标准状况下,22.4L氖气中含有原子数为2NA | |
| C. | 28g CO和N2混合气体含有的原子数为2NA | |
| D. | 2mol钠与足量O2完全反应生成Na2O2时失去电子数为NA |
分析 A. 12C中含有6个中子,根据n=$\frac{m}{M}$计算出碳原子的物质的量,然后计算出含有中子数;
B.氖气为单原子分子,1mol氖气分子中含有1mol氖原子;
C.二者摩尔质量都是28g/mol,且为双原子分子,根据n=$\frac{m}{M}$计算混合物中含有原子的物质的量及数目;
D.钠为+1价金属,2mol钠完全反应失去2mol电子.
解答 解:A.12g 12C的物质的量为:$\frac{12g}{12g/mol}$=1mol,1mol该碳原子中含有6mol中子,含有中子数为6NA,故A错误;
B.标况下22.4L氖气的物质的量为1mol,1mol氖气分子中含有1mol氖原子,含有原子数为NA,故B错误;
C.28g CO和N2混合气体中含有气体的物质的量为:$\frac{28g}{28g/mol}$=1mol,1mol该混合气体中含有2mol原子,含有的原子数为2NA,故C正确;
D.金属Na为+1价金属,2mol钠与足量O2完全反应生成Na2O2时失去2mol电子,失去电子数为2NA,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的计算与判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,B为易错点,注意稀有气体为单原子分子,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.研究发现,烯烃在合适催化剂作用下可双键断裂,两端基团重新组合为新的烯烃.若CH2=C(CH3)CH2CH3与CH2=CHCH2CH3的混合物发生该类反应,则新生成的烯烃中一定共平面的碳原子数可能为( )
| A. | 2,4,5,6 | B. | 3,4,5,6 | C. | 2,3,4,5 | D. | 4,5,6,7 |
5.下列不能用勒夏特列原理解释的是( )
| A. | 热的纯碱溶液去油污效果好 | |
| B. | 新制的氯水在光照条件下颜色变浅 | |
| C. | 收集氯气用排饱和食盐水的方法 | |
| D. | 500℃左右比室温更有利于合成氨的反应 |
12.工业上曾用电解60%硫酸溶液(或硫酸氢钾、硫酸氢铵浓溶液)制取过氧化氢,其生产流程如图:

下列说法错误的是( )

下列说法错误的是( )
| A. | 电解硫酸或酸式硫酸盐溶液,阳极反应为2SO42--2e-═S2O82- | |
| B. | S2O82-具有强氧化性,H2S2O8是二元强酸 | |
| C. | 减压蒸馏的目的是为了减少H2O2分解,蒸馏得到的另一组分可循环利用 | |
| D. | 由溶液A转化为溶液B发生了氧化还原反应 |
9.反应Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$ CuSO4+SO2↑+2H2O中,还原产物是( )
| A. | CuSO4 | B. | H2SO4 | C. | H2O | D. | SO2 |
7.物质的检验、鉴别要特别注意到共存物质的干扰,否则得到的结论就是不可靠的,例如,实验室用乙醇、浓硫酸在170℃时制得的CH2=CH2 中混有SO2,用溴水或酸性KMnO4溶液检验生成的CH2=CH2时,就要考 虑到SO2 的影响,因为SO2也能使溴水或酸性KMnO4溶液褪色,所以检验有CH2=CH2生成就需先除去SO2.下列实验设计所得结论可靠的是( )
| A. | 将电石与水反应产生的气体通入酸性KMnO4溶液中,溶液褪色说明有乙炔生成 | |
| B. | 将溴乙烷与NaOH 的乙醇溶液共热产生的气体通入到酸性KMnO4溶液中,溶液褪色说明有CH2=CH2生成 | |
| C. | 将溴乙烷与NaOH 的乙醇溶液共热产生的气体通入到溴水中,溴水褪色,说明有乙烯生成 | |
| D. | 将苯、液溴、铁粉混合物反应产生的气体通入到AgNO3溶液中有淡黄色沉淀产生,说明有HBr 生成 |

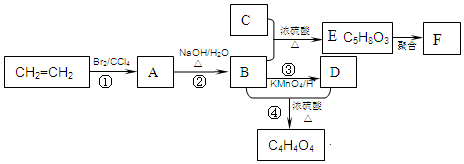
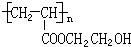 .
.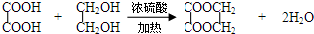 .
.