题目内容
W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如图所示,已知W的一种核素的质量数为18 ,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大.请回答下列问题:
,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大.请回答下列问题:
(1)X元素位于元素周期表中第 周期 族.
(2)X的单质和Y的单质相比,熔点较高的是 (写化学式);Z的气态氢化物和溴化氢相比.较稳定的是 (写化学式).
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是 .
 ,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大.请回答下列问题:
,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的吸引电子的能力在同周期主族元素中最大.请回答下列问题:(1)X元素位于元素周期表中第
(2)X的单质和Y的单质相比,熔点较高的是
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
考点:位置结构性质的相互关系应用
专题:
分析:W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,则其质子数为18-10=8,故W为O元素;X和Ne原子的核外电子数相差1,原子半径大于O,故X为Na;由原子序数可知,Y、Z处于第三周期,而Y的单质是一种常见的半导体材料,则Y为Si,Z的吸引电子的能力在同周期主族元素中最大,则Z为Cl,据此解答.
解答:
解:W、X、Y、Z是四种常见的短周期元素,W的一种核素的质量数为18,中子数为10,则其质子数为18-10=8,故W为O元素;X和Ne原子的核外电子数相差1,原子半径大于O,故X为Na;由原子序数可知,Y、Z处于第三周期,而Y的单质是一种常见的半导体材料,则Y为Si,Z的吸引电子的能力在同周期主族元素中最大,则Z为Cl,
(1)X为Na元素,位于元素周期表中第三周期IA族,故答案为:三、IA;
(2)金属Na的熔点较低,Si属于原子晶体,熔点很高,故Si的熔点较高;非金属性Cl>Br,故氢化物稳定性HCl>HBr,故答案为:Si;HCl;
(3)Y与Z形成的化合物为SiCl4,和足量水反应,生成一种弱酸和一种强酸,应生成H4SiO4与HCl,该反应的化学方程式是:SiCl4+4H2O=H4SiO4+4HCl,故答案为:SiCl4+4H2O=H4SiO4+4HCl.
(1)X为Na元素,位于元素周期表中第三周期IA族,故答案为:三、IA;
(2)金属Na的熔点较低,Si属于原子晶体,熔点很高,故Si的熔点较高;非金属性Cl>Br,故氢化物稳定性HCl>HBr,故答案为:Si;HCl;
(3)Y与Z形成的化合物为SiCl4,和足量水反应,生成一种弱酸和一种强酸,应生成H4SiO4与HCl,该反应的化学方程式是:SiCl4+4H2O=H4SiO4+4HCl,故答案为:SiCl4+4H2O=H4SiO4+4HCl.
点评:本题考查位置结构性质关系等,难度中等,推断元素是解题的关键,注意对元素周期律的理解与运用.

练习册系列答案
 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
不粘锅的内壁有一薄层为聚四氟乙烯的高分子材料涂层,用不粘锅烹烧菜时不易粘锅、烧焦.下列关于聚四氟乙烯的说法正确的是( )
| A、聚四氟乙烯分子中含有双键 |
| B、聚四氟乙烯的单体是不饱和烃 |
| C、聚四氟乙烯中氟的质量分数是76% |
| D、聚四氟乙烯的化学性质活泼 |
下列各物质的电子式书写错误的是( )
A、 |
B、 |
C、 |
D、 |
下列有关核外电子运动规律的描述中,错误的是( )
| A、核外电子质量很小,在原子核外做高速运动 |
| B、在电子云示意图中,小黑点密表示电子在核外空间单位体积内出现的几率大 |
| C、在电子云示意图中,通常用小黑点来表示电子绕核做高速圆周运动 |
| D、s电子的原子轨道都是球形的,p电子的原子轨道都是哑铃形的 |
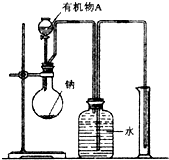 26.4g某液态有机化合物A完全燃烧后,生成21.6g H2O和52.8gCO2.测得有机化合物A的蒸气对H2的相对密度是44,求:
26.4g某液态有机化合物A完全燃烧后,生成21.6g H2O和52.8gCO2.测得有机化合物A的蒸气对H2的相对密度是44,求: