题目内容
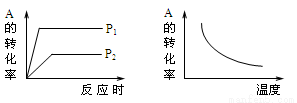
对于可逆反应:mA(g)+nB(g) 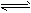 xC(g) ΔH,在不同温度及压强(P1、P2)条件下,反应物A的转化率如图所示,下列判断正确的是
xC(g) ΔH,在不同温度及压强(P1、P2)条件下,反应物A的转化率如图所示,下列判断正确的是
A.ΔH<0,m+n>x B.ΔH>0,m+n<x
C.ΔH<0,m+n<x D.ΔH>0,m+n>x
A
【解析】
试题分析:由压强对平衡的影响图像可以看出,P1条件下反应先达平衡,P1>P2 ,压强增大,A的转化率增大,平衡向正方向移动,m+n>x ,温度升高,A的转化率减小,平衡向逆反应方向移动,正反应放热,ΔH<0,答案选A。
考点:化学平衡的图像

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案 天天练口算系列答案
天天练口算系列答案
相关题目
下列叙述I和II均正确并有因果关系的是
选项 | 叙述I | 叙述II |
A | 实验室常用Al2(SO4)3溶液与氨水溶液制备Al(OH)3沉淀 | Al(OH)3不溶于碱 |
B | NaHCO3为强碱弱酸盐 | NaHCO3 溶液显碱性 |
C | SO2具有氧化性 | SO2可用品红溶液检验 |
D | Fe(OH)3胶体有丁达尔效应 | Fe(OH)3胶体可以用FeCl3浓溶液与NaOH溶液反应制得 |
相同温度下,体积均为0.25L的两个恒容密闭容器中发生可逆反应:N2 (g)+3H2 (g)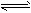 2NH3 (g),△H= - 92. 6kJ/moL。实验测得起始、平衡时的有关数据如下表:
2NH3 (g),△H= - 92. 6kJ/moL。实验测得起始、平衡时的有关数据如下表:
容器编号 | 起始时各物质物质的量/mol | 达平衡时体系 能量的变化 | ||
N2 | H2 | NH3 | ||
① | 1 | 3 | 0 | 放出热量:23.15kJ |
② | 0.9 | 2.7 | 0.2 | 放出热量:Q |
下列叙述错误的是
A.容器②中达平衡时放出的热量Q=23. 15kJ
B.平衡时,两个容器中NH3的体积分数均为1/7
C.容器①、②中反应的平衡常数相等
D.若容器①体积为0.5L,则平衡时放出的热量小于23. 15kJ
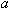 g,一个12C的原子质量是b g,用NA是阿伏加德罗常数的值,下列叙述中不正确的是
g,一个12C的原子质量是b g,用NA是阿伏加德罗常数的值,下列叙述中不正确的是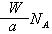 个原子
个原子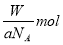 D.由已知信息可得:
D.由已知信息可得: mol-1
mol-1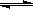 2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是
2C(g)+2D(g),在不同情况下测得反应速率如下,其中反应速率最快的是