题目内容
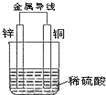 关于如图所示装置的叙述,对其描述正确的是( )
关于如图所示装置的叙述,对其描述正确的是( )分析:根据原电池工作原理判断正负极、电极反应现象、溶液中离子的移动方向、电子的流向、溶液中离子的浓度是否变化、电极反应式.
解答:解:A、锌片、铜片和稀硫酸溶液构成的原电池中,铜作正极,正极上氢离子得电子生成氢气,故A错误;
B、原电池是将化学能转变为电能的装置,故B错误;
C、锌失电子通过导线流向铜,所以电子流向为由Zn经导线流入Cu片,即从负极通过导线流向正极,故C正确;
D、铜作正极,正极上氢离子得电子生成氢气,发生还原反应,电极反应式为2H++2e-=H2↑,故D错误.
故选C.
B、原电池是将化学能转变为电能的装置,故B错误;
C、锌失电子通过导线流向铜,所以电子流向为由Zn经导线流入Cu片,即从负极通过导线流向正极,故C正确;
D、铜作正极,正极上氢离子得电子生成氢气,发生还原反应,电极反应式为2H++2e-=H2↑,故D错误.
故选C.
点评:本题考查学生原电池的工作原理知识,可以根据所学知识进行回答,难度不大.

练习册系列答案
相关题目
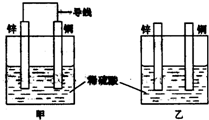 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )| A、两装置中锌片都发生氧化反应 | B、两装置中溶液的pH均增大 | C、两装置中铜片的质量均逐渐减小 | D、两装置中铜片表面均无气泡产生 |

 关于如图所示装置的叙述正确的是( )
关于如图所示装置的叙述正确的是( )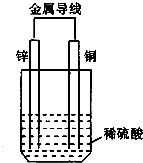
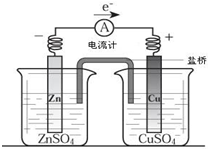 关于如图所示装置的叙述,正确的是( )
关于如图所示装置的叙述,正确的是( )