题目内容
14.已知阿伏加德罗常数的值为NA,则下列说法正确的是( )| A. | 1 mol/L CuCl2溶液中含有的Cl-的个数为2NA | |
| B. | 16 g甲烷中含有的共用电子对数为NA | |
| C. | 常温常压,46 gNO2与N2O4的混合气体中含有的原子数为3NA | |
| D. | 4.6 g Na与适量氧气完全反应生成Na2O、Na2O2的混合物中含有的阴离子数大于0.1NA |
分析 A、溶液体积不明确;
B、求出甲烷的物质的量,然后根据1mol甲烷中含4mol共价键来分析;
C、NO2与N2O4的最简式均为NO2;
D、求出钠的物质的量,然后根据钠反应后生的氧化钠和过氧化钠均由2个钠离子和1个阴离子构成来分析.
解答 解:A、溶液体积不明确,故溶液中的氯离子的个数无法计算,故A错误;
B、16g甲烷的物质的量为1mol,而1mol甲烷中含4mol共价键,故含4NA对共用电子对,故B错误;
C、NO2与N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为1mol,则含有3NA个原子,故C正确;
D、4.6g钠的物质的量为0.2mol,反应后生成0.2mol钠离子,而钠反应后生的氧化钠和过氧化钠均由2个钠离子和1个阴离子构成,故0.2molNa+所对应的阴离子为0.1NA个,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.表示阿伏加德罗常数,下列说法正确的是( )
| A. | 0.5molAl与足量盐酸反应转移电子数为1NA | |
| B. | 标准状况下22.4LH2中含中子数为2 NA | |
| C. | 0.5mol CH4所含电子数为5 NA | |
| D. | 1L1 mol/L醋酸溶液中离子总数为2 NA |
5.下列营养素中,不能对人体提供能量的是( )
| A. | 蛋白质 | B. | 糖类 | C. | 维生素 | D. | 油脂 |
9.下列有机反应中,属于加成反应的是( )
| A. | C6H12O6$\stackrel{酒化酶}{→}$2C2H6O+2CO2↑ | B. | CH4+Cl2$\stackrel{光照}{→}$CH3Cl+HCl | ||
| C. | HC≡CH+HCl$\stackrel{一定条件}{→}$CH2=CHCl | D. | 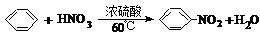 |
19.已知下述三个实验均能发生化学反应.
下列判断正确的是( )
| ① | ② | ③ |
| 将铁钉放入硫酸铜溶液中 | 向硫酸亚铁溶液中滴入几滴浓硝酸 | 将铁钉放入氯化铁溶液中 |
| A. | 实验①和③中的铁钉只作还原剂 | |
| B. | 上述实验证明氧化性:Fe3+>Fe2+>Cu2+ | |
| C. | 实验②中,当转移0.2mol电子时,有0.1mol的Fe2+被氧化 | |
| D. | 实验③中反应的离子方程式为:Fe+Fe3+═2Fe2+ |
6.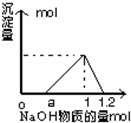 往Al2(SO4)3与H2SO4混合溶液中逐滴加入NaOH溶液,所得沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则Al2(SO4)3与H2SO4的物质的量浓度之比为( )
往Al2(SO4)3与H2SO4混合溶液中逐滴加入NaOH溶液,所得沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则Al2(SO4)3与H2SO4的物质的量浓度之比为( )
 往Al2(SO4)3与H2SO4混合溶液中逐滴加入NaOH溶液,所得沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则Al2(SO4)3与H2SO4的物质的量浓度之比为( )
往Al2(SO4)3与H2SO4混合溶液中逐滴加入NaOH溶液,所得沉淀的物质的量与加入NaOH的物质的量的关系如图所示,则Al2(SO4)3与H2SO4的物质的量浓度之比为( )| A. | 1:3 | B. | 1:4 | C. | 1:1 | D. | 1:2 |
4.下列离子方程式正确的是( )
| A. | 向CuSO4溶液中投入Na:Cu2++2Na═Cu+2Na+ | |
| B. | 向FeCl3溶液中滴加KSCN溶液:Fe3++3SCN-═Fe(SCN)3↓ | |
| C. | 用氨水溶解Cu(OH)2:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++2OH-+4H2O | |
| D. | 向BaCO3固体中加入过量的稀H2SO4:BaCO3+2H+═Ba2++CO2↑+H2O |