题目内容
钢铁在潮湿的空气中会被腐蚀,会发生的原电池反应.以下说法正确的是( )
| A、负极发生的反应为:Fe-3e-=Fe3+ |
| B、正极发生的反应为:2H2O+O2+4e-=4OH? |
| C、原电池是将电能转变为化学能的装置 |
| D、钢铁在水下部分比在空气与水交界处更容易腐蚀 |
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:根据原电池的定义、原电池的电极反应式、以及氧气的溶解度判断,钢铁在潮湿的空气中会被腐蚀,发生的原电池反应为:2Fe+2H2O+O2═2Fe(OH)2是发生的吸氧腐蚀,原电池中负极发生氧化反应,正极发生还原反应.
解答:
解:钢铁中含有铁和碳,在潮湿的环境中构成原电池,铁作负极,碳作正极.
A、根据反应方程式知,负极反应式为Fe-2e-=Fe2+,故A错误;
B、正极上氧气得电子生成氢氧根离子,则正极发生的反应为:2H2O+O2+4e-=4OH-,故B正确;
C、原电池是将化学能转变为电能的装置,故C错误;
D、氧气在水中的溶解度较小,在水下部分比在空气与水交界处更难腐蚀,故D错误;
故选B.
A、根据反应方程式知,负极反应式为Fe-2e-=Fe2+,故A错误;
B、正极上氧气得电子生成氢氧根离子,则正极发生的反应为:2H2O+O2+4e-=4OH-,故B正确;
C、原电池是将化学能转变为电能的装置,故C错误;
D、氧气在水中的溶解度较小,在水下部分比在空气与水交界处更难腐蚀,故D错误;
故选B.
点评:本题考查了金属的腐蚀与防护,明确形成原电池的条件及原电池原理是解本题关键,会根据环境确定钢铁发生吸氧腐蚀还是析氢腐蚀,会书写电极反应式,为学习难点.

练习册系列答案
相关题目
同温同压下,已知下列各反应为放热反应,下列各热化学方程式中△H最小的是( )
| A、2A (l)+B (l)=2C (g)△H1 |
| B、2A (g)+B (g)=2C(g)△H2 |
| C、2A (g)+B (g)=2C (l)△H3 |
| D、2A (l)+B (l)=2C(l)△H4 |
下列有关电解质的叙述中正确的是( )
| A、二氧化碳溶于水可以导电,所以二氧化碳属于电解质 |
| B、在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质 |
| C、只有酸碱盐才是电解质 |
| D、纯净的电解质在液态时,有的导电,有的不导电 |
下列事实不能用电化学原理解释的是( )
| A、实验室制氢气时用粗锌比用纯锌放出氢气快 |
| B、镀锌铁(在铁上镀一层锌)比镀锡铁耐腐蚀 |
| C、铝制门窗不用涂刷油漆 |
| D、轮船水线以下的船壳上装一定数量的锌块 |
NA表示阿伏加德罗常数,下列说法错误的是( )
| A、56g铁与足量的氯气反应,转移电子数为3NA |
| B、常温常压下,22.4L甲烷所含的电子数为10NA |
| C、常温常压下,34g氨气所含的原子数为8NA |
| D、NA个氧分子和NA个氢分子的质量比为16:1 |
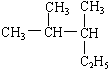 用系统命名法命名
用系统命名法命名 中含有的官能团的名称为
中含有的官能团的名称为