题目内容
9.在密闭容器中发生化学反应H2(g)+I2(g)?2HI(g),0?5min内H2的浓度减少了0.1mol/L,则在这段时间内,用HI表示的平均反应速率为( )| A. | 0.01mol•L-1•min-1 | B. | 0.2mol•L-1•min-1 | ||
| C. | 0.04mol•L-1•min-1 | D. | 0.5mol•L-1•min-1 |
分析 根据氢气的物质的量浓度的变化计算HI的浓度变化,结合c=$\frac{△c}{△t}$计算.
解答 解:0~5min内H2的浓度减少了0.1mol/L,由方程式可知△c(HI)=2△c(H2)=0.2mol/L,
v(HI)=$\frac{0.2mol/L}{5min}$=0.04mol/(L•min),
故选C.
点评 本题考查化学反应速率的相关计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握化学反应速率的定义以及计算公式,难度不大.

练习册系列答案
相关题目
19. 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )
 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )
如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,这些记录中合理的是( )| A. | 铜是负极,锌为正极 | |
| B. | 铜表面产生大量气体 | |
| C. | 正极反应式:Cu-2e-═Cu2+,发生氧化反应 | |
| D. | 导线中电子的流向是:Cu→Zn |
20.下列实验操作方法正确的是( )
| A. | 欲除去乙烷中混有的乙烯可选用酸性KMnO4溶液洗气 | |
| B. | 使用萃取的方法可提纯粗苯甲酸 | |
| C. | 欲区分苯和甲苯,分别取少量样品加足量酸性KMnO4溶液,振荡,KMnO4溶液褪色为甲苯,反之为苯 | |
| D. | 欲确定溴乙烷中含有溴原子,加入适量NaOH溶液后加热,待溶液冷却后滴加AgNO3溶液,若生成淡黄色沉淀即可确定 |
17.下列实验误差分析错误的是( )
| A. | 用润湿的pH试纸测稀碱溶液的pH,测定值偏小 | |
| B. | 容量瓶中含有少量蒸馏水对所配制的溶液无影响 | |
| C. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| D. | 测定中和反应的中和热时,保温效果越好,测定误差越小 |
4.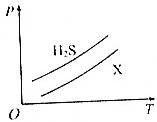 如图所示,表示1 g H2S与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
如图所示,表示1 g H2S与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
 如图所示,表示1 g H2S与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )
如图所示,表示1 g H2S与1g X气体在相同容积的密闭容器中压强(p)与温度(T)的关系,则X气体可能是( )| A. | N2 | B. | CH4 | C. | NO | D. | SO2 |
14.将下列各种液体分别与溴水混合并振荡,静置后混合液分为两层,溴水层几乎无色的是( )
| A. | 苯 | B. | 酒精 | C. | 碘化钾溶液 | D. | 己烷 |
1.下列关于SO2的叙述中,正确的是( )
| A. | 可以用碱石灰来干燥SO2气体 | |
| B. | 通入BaCl2溶液中,无明显现象 | |
| C. | 因为SO2有漂白性,所以它能使品红溶液、溴水褪色 | |
| D. | 将1.12L的SO2气体通入装有100mL 1mol/L的FeCl3溶液的试管里,恰好完全反应 |
3.下列说法正确的是( )
| A. | 分子式为C8H10的芳香化合物有3种可能的不同结构 | |
| B. | 分子式为C4H9Cl的有机物有3种可能的不同结构 | |
| C. | 分子式为C4H8属于烯烃的有机物有3种可能的不同结构 | |
| D. | 分子式为C5H12的有机物有4种可能的不同结构 |
 .
.