题目内容
计算题
碳在一定量空气中燃烧,生成混合气体标准状况下为6.72L,总质量为10.8g.
则生成的气体可能含 , .
求:(1)混合气体中各气体的物质的量是多少?
(2)将混合气体通入2L 0.1mol/L的NaOH溶液中恰好完全反应(忽略体积变化),生成碳酸钠和碳酸氢钠,请问溶液中两物质的物质的量浓度为?
碳在一定量空气中燃烧,生成混合气体标准状况下为6.72L,总质量为10.8g.
则生成的气体可能含
求:(1)混合气体中各气体的物质的量是多少?
(2)将混合气体通入2L 0.1mol/L的NaOH溶液中恰好完全反应(忽略体积变化),生成碳酸钠和碳酸氢钠,请问溶液中两物质的物质的量浓度为?
考点:有关混合物反应的计算
专题:计算题
分析:碳在一定的空气中燃烧生成的混合气体为CO、CO2;
(1)设CO、CO2的物质的量分别为xmol、ymol,根据二者体积及质量列方程计算各自物质的量;
(2)氢氧化钠溶液吸收二氧化碳,设生成Na2CO3、NaHCO3的物质的量分别为amol、bmol,根据C元素守恒、钠离子守恒列方程计算解答.
(1)设CO、CO2的物质的量分别为xmol、ymol,根据二者体积及质量列方程计算各自物质的量;
(2)氢氧化钠溶液吸收二氧化碳,设生成Na2CO3、NaHCO3的物质的量分别为amol、bmol,根据C元素守恒、钠离子守恒列方程计算解答.
解答:
解:碳在一定的空气中燃烧生成的混合气体为CO、CO2,故答案为:CO、CO2;
(1)设CO、CO2的物质的量分别为xmol、ymol,根据二者体积及质量列方程,则:
解得x=0.15 y=0.15
答:混合气体中CO为0.15mol,CO2,为0.15mol;
(2)氢氧化钠溶液吸收二氧化碳,设生成Na2CO3、NaHCO3的物质的量分别为amol、bmol,根据C元素守恒、钠离子守恒列方程,则:
解得a=0.05 b=0.1
则c(Na2CO3)=
=0.025mol/L
c(NaHCO3)=
=0.05mol/L,
答:溶液中碳酸钠为0.025mol/L,碳酸氢钠为0.05mol/L.
(1)设CO、CO2的物质的量分别为xmol、ymol,根据二者体积及质量列方程,则:
|
解得x=0.15 y=0.15
答:混合气体中CO为0.15mol,CO2,为0.15mol;
(2)氢氧化钠溶液吸收二氧化碳,设生成Na2CO3、NaHCO3的物质的量分别为amol、bmol,根据C元素守恒、钠离子守恒列方程,则:
|
解得a=0.05 b=0.1
则c(Na2CO3)=
| 0.05mol |
| 2L |
c(NaHCO3)=
| 0.1mol |
| 2L |
答:溶液中碳酸钠为0.025mol/L,碳酸氢钠为0.05mol/L.
点评:本题考查混合物计算,难度不大,注意利用方程组进行解答.

练习册系列答案
 学习实践园地系列答案
学习实践园地系列答案
相关题目
将下列离子方程式改写成化学方程式,正确的是( )
| A、Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 |
| B、CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O |
| C、Ca2++CO32═CaCO3↓ CaCl2+Na2CO3═CaCO3↓+2NaCl |
| D、H++OH-═H2O NaOH+H2CO3=NaHCO3+H2O |
解释下列现象的化学用语不正确的是( )
| A、铁钉在空气中出现红色的铁锈,其负极反应式为:Fe-3e-═Fe3+ |
| B、氢氧化镁白色沉淀溶于氯化铵溶液:Mg(OH)2+2NH4+═Mg2++2NH3?H2O |
| C、向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+2AlO2-+2H2O |
| D、漂白粉溶液中加氯化铁溶液产生大量红褐色沉淀:Fe3++3ClO-+3H2O═Fe(OH)3↓+3HClO |
 如图:纵坐标表示可燃气体A、B、C(C是A和B的混合物)的体积,横坐标表示A、B、C在完全燃烧时,消耗O2的体积,测混合气体C中A和B的体积比为( )
如图:纵坐标表示可燃气体A、B、C(C是A和B的混合物)的体积,横坐标表示A、B、C在完全燃烧时,消耗O2的体积,测混合气体C中A和B的体积比为( )| A、VA:VB=1:1 |
| B、VA:VB=1:2 |
| C、VA:VB=2:1 |
| D、VA:VB为任意比 |
中学阶段介绍的应用电解法制备的物质主要有三种:一是铝的工业制备、二是氯碱工业、三是金属钠或镁的制备.下列关于这三个工业生产的描述中正确的是( )
| A、电解法制镁时一般是用熔融态的氯化镁进行电解,但也可用其相应的盐,如熔融态的碳酸镁 |
| B、电解法生产铝时,需对铝土矿进行提纯,在提纯过程中应用了氧化铝或氢氧化铝的两性 |
| C、在氯碱工业中,电解池中的阴极产生的是H2,NaOH在阳极附近产生 |
| D、氯碱工业和金属钠的冶炼都用到了NaCl,在电解时它们的阴极都是Cl-失电子 |
用惰性电极电解200mLCuSO4溶液.通电一段时间后,测定两极均产生224mL气体(已换算至标准状况下,且忽略溶液体积的变化及气体在溶液中的溶解),则原溶液中溶质的物质的量浓度和所得溶液的pH为( )
| A、0.04 mol?L-1 1 |
| B、0.02 mol?L-1 2 |
| C、0.03 mol?L-1 5 |
| D、0.05mol?L-1 1 |
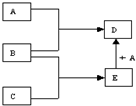 已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略).
已知A、B、C、D、E均为常见物质,在一定条件下相互转化关系如图所示(反应条件和部分产物已省略). 某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是探究了碳酸氢钠的化学性质.
某化学兴趣小组的同学在学习了纯碱(Na2CO3)的性质后,联想到家中蒸制馒头时常用的物质小苏打(NaHCO3),于是探究了碳酸氢钠的化学性质.