题目内容
16.水处理技术在生产、生活中应用广泛.(1)根据水中Ca2+、Mg2+的多少,把天然水分为硬水和软水,硬水必须经过软化才能使用.
①硬水软化的方法通常有热煮沸法、药剂法和离子交换法.离子交换树脂使用了一段时间后,逐渐由NaR型变为CaR2(或MgR2)型,而失去交换能力.把CaR2(或MgR2)型树脂置于5%-8%的食盐水中浸泡一段时间,便可再生.
②当洗涤用水硬度较大时,洗衣粉与肥皂相比,洗衣粉洗涤效果较好,原因是肥皂易与Ca2+,Mg2+生成沉淀.
(2)工业上常用绿矾做混凝剂除去天然水中含有的悬浮物和胶体,为了达到更好的效果,要将待处理的水pH调到9左右,再加入绿矾.请解释这一做法的原因:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体).(用必要的离子方程式和文字描述).
(3)最近我国某地苯胺大量泄漏于生活饮用水的河道中,当地采取的应急措施之一是向河水中撒入大量的活性炭,活性炭的作用是吸附泄漏在河水中的有机物.
分析 (1)①硬水软化的方法通常有①热煮沸法②药剂软化法③蒸馏法④离子交换法⑤电渗析法⑥离子膜电解法;
用磺化煤(NaR)作离子交换剂:2NaR+Ca2+=CaR2+2Na+,2NaR+Mg2+=MgR2+2Na+,用5%-8%的食盐水浸泡可使失去软化能力的磺化煤再生:CaR2+2Na+=2NaR+Ca2+,MgR2+2Na+=2NaR+Mg2+;
②肥皂易与Ca2+,Mg2+生成沉淀,洗涤效果不好;
(2)由于FeSO4•7H2O溶于水后显酸性,而Fe2+在碱性条件下更容易被氧化成Fe3+,所以要将pH调到9左右,变成效果更好的三价铁离子;
(3)活性炭具有吸附性,以此来解答.
解答 解:(1)①硬水软化的方法通常有①热煮沸法②药剂软化法③蒸馏法④离子交换法⑤电渗析法⑥离子膜电解法;用磺化煤(NaR)作离子交换剂:2NaR+Ca2+=CaR2+2Na+,2NaR+Mg2+=MgR2+2Na+,用5%-8%的食盐水浸泡可使失去软化能力的磺化煤再生:CaR2+2Na+=2NaR+Ca2+,MgR2+2Na+=2NaR+Mg2+;
故答案为:热煮沸法;药剂法;5%-8%的食盐水;
②肥皂易与Ca2+,Mg2+生成硬脂酸钙、硬脂酸镁沉淀,洗涤效果不好,洗衣粉不与Ca2+,Mg2+生成沉淀,洗涤效果较好,
故答案为:洗衣粉;肥皂易与Ca2+,Mg2+生成沉淀;
(2)Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)胶体,起到较好的混凝作用,发生的离子反应为4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体),
故答案为:Fe2+在碱性条件下易被氧化成Fe3+,进而水解生成Fe(OH)胶体,起到较好的混凝作用,4Fe2++O2+2H2O+8OH-=4Fe(OH)3(胶体);
(3)活性炭具有吸附性,能吸附泄露在河水中的有机物,故答案为:吸附泄漏在河水中的有机物.
点评 本题考查混合物分离提纯及污水处理,为高频考点,把握物质的性质及混合物分离方法等为解答的关键,侧重分析与实验能力的考查,注重化学与生活的关系,题目难度不大.

| A. | 5.6 g铁粉与硝酸反应失去电子数一定为0.3×6.02×1023 | |
| B. | 反应MgCl2(s)═Mg(s)+Cl2(g)的△H<0、△S>0 | |
| C. | Ksp不仅与难溶电解质的性质和温度有关,还与溶液中相关离子的浓度有关 | |
| D. | 0.1 mol•L-1 Na2SO3溶液中:c(OH-)-c(H+)=2c(H2SO3)+c(HS${o}_{3}^{-}$) |
| A. | 单位时间内消耗amolD,同时生成2amolC | |
| B. | 3v(B)正=2v(C)逆 | |
| C. | 容器内的压强不再变化 | |
| D. | C(B);C(C);C(D)=3;2;1 |
 W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大.W,Z同主族,可形成离子化合物ZW;Y,M同主族,可形成MY2,MY3两种分子;X的气态氢化物水溶液呈碱性.请回答下列问题:
(1)Y在元素周期表中的位置为第二周期第VIA族;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是HClO4(写化学式)
(3)W、Y、Z、G形成的简单离子的半径大小顺序是Cl->N3->O2->Na+(用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有O3、Cl2、ClO2 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是H2S(填化学式),沸点高的是H2O(填化学式)
(6)ZW的电子式为Na+[:H]-,W2Y2的电子式为
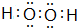 ,用电子式表示Z2M的形成过程:
,用电子式表示Z2M的形成过程: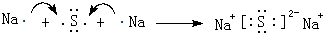 .
.(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液不褪色(填“褪色”或“不褪色”),请用相关离子方程式解释原因SO2+Cl2+2H2O=SO42-+2Cl-+4H+.
(8)已知
| 化合物 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 类型 | 离子化合物 | 离子化合物 | 离子化合物 | 共价化合物 |
| 熔点/℃ | 2800 | 2050 | 714 | 191 |
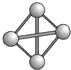
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子.N4分子结构如图所示,已知断裂1mol N-N吸收167kJ热量,生成1mol N≡N入出942kJ.根据以上信息和数据,下列说法正确的是C.
A.N4属于一种新型化合物
B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2
D.1molN4转变为N2将吸收882KJ的能量.
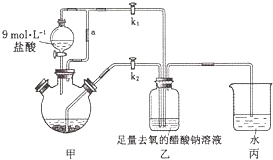

 )和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式:
)和双氧水为原料生产过氧化苯甲酰,写出合成过氧化苯甲酰的化学反应方程式: ,该反应属于取代反应.
,该反应属于取代反应.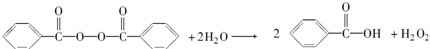 .苯甲酸的同分异构体中,属于酯类的有
.苯甲酸的同分异构体中,属于酯类的有 ,属于酚类的有3.(写结构简式)
,属于酚类的有3.(写结构简式)