题目内容
反应2SO2+O2?2SO3经一段时间后,SO2的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L?s).则这段时间为( )
| A、0.1s | B、2.5s |
| C、5s | D、10s |
考点:反应速率的定量表示方法
专题:
分析:根据速率之比等于化学计量数之比计算v(SO3),再利用△t=
进行计算.
| △c |
| v |
解答:
解:用O2表示的反应速率为0.04mol/(L?s),
则v(SO3)=2v(O2)=2×0.04mol/(L?s)=0.08mol/(L?s),
故反应时间=
=5s,
故选C.
则v(SO3)=2v(O2)=2×0.04mol/(L?s)=0.08mol/(L?s),
故反应时间=
| 0.4mol/L |
| 0.08mol/(L.s) |
故选C.
点评:本题考查化学反应速率的有关计算,比较基础,注意对公式的理解与灵活运用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
室温下,下列各组离子在指定溶液中一定大量共存的是( )
| A、在NaHCO3溶液中:K+、Cl-、CH3COO-、C6H5O- |
| B、在pH=13的无色溶液中:K+、Na+、I-、Cr2O72- |
| C、甲基橙黄色的溶液中:Na+、Al3+、NO3-、F- |
| D、1.0mol?L-1的KCl的溶液中:H+、Ag+、SO42-、NO3- |
下列关于苯的说法中,正确的是( )
| A、苯的密度比水大 |
| B、能用酸性高锰酸钾溶液鉴别苯和甲苯 |
| C、苯环上存在碳碳单键和碳碳双键交替出现的结构 |
| D、苯能发生取代反应但不能发生加成反应 |
可逆反应:2NO?2NO+O2在体积固定的密闭容器中进行,下列说法不能认为达到平衡状态的是( )
| A、单位时间内生成 n mol的O2同时生成2n molNO2 |
| B、混合气体的颜色不再改变的状态 |
| C、混合气体的密度不再改变的状态 |
| D、混合气体的压强不再改变的状态 |
500K时,有CO催化剂加氢反应:CO(g)+3H2(g)?CH4(g)+H2O(g)△H<0,下列有关说法正确的是( )
| A、温度升高时,该反应的平衡常数K增大 |
| B、缩小容器体积,平衡体系中各物质的浓度均增大 |
| C、温度越低,越有有利于CO催化氢 |
| D、从平衡体系中分离出H2O(g)能加快正反应速率 |
在相同条件下,下列两个反应的反应热分别以△H1和△H2表示:(1)2H2(气)+02(气)=2H20(气);△H1
(2)2H2 (气)+02(气)=2H2O(液);△H2;△H1和AH2的关系为( )
(2)2H2 (气)+02(气)=2H2O(液);△H2;△H1和AH2的关系为( )
| A、△H1>△H2 |
| B、△H1<△H2 |
| C、△H1=△H2 |
| D、无法确定 |
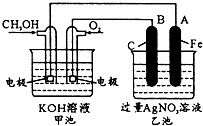 如图是一个化学过程的示意图.已知甲池的总反应式为:
如图是一个化学过程的示意图.已知甲池的总反应式为: