题目内容
计算:某温度时,测得0.01mol/L的NaOH溶液pH为11,则该温度下水的离子积常数Kw= .
考点:离子积常数
专题:
分析:依据Kw=[H+][OH-],pH=-lg[H+],分别计算出氢离子和氢氧根离子浓度,然后计算解答;
解答:
解:氢氧化钠为强电解质,完全电离,所以0.01mol/L的氢氧化钠中,C(OH-)=10-2mol/L;因为pH=-lg[H+],所以C(H+)=10-11mol/L,所以Kw=c(H+)×c(OH-)=1×10-13,
故答案为:1×10-13.
故答案为:1×10-13.
点评:本题考查了水的离子积常数的应用,为高考热门考点,题目难度中等.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
相关题目
化学与日常生活密切相关,下列说法错误的是( )
| A、碘酒是指单质碘的乙醇溶液 |
| B、84消毒液的有效成分是NaClO |
| C、生石灰用作食品抗氧剂 |
| D、小苏打是面包发酵粉的主要成分 |
将25%的硫酸溶液和5%的硫酸溶液等体积混合,所得硫酸溶液的质量分数是( )
| A、等于15% | B、大于15% |
| C、小于15% | D、无法估算 |
下列做法体现了环境保护理念的有( )
| A、大力推广使用含甲醛涂料 |
| B、研究开发可降解塑料 |
| C、燃烧废旧电线提取铜线 |
| D、将实验室废液集中进行无害化处理 |
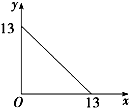 T℃下的溶液中,c(H+)=1.0×10-xmol?L-1,c(OH-)=1.0×10-ymol?L-1,x与y的关系如图所示.下列说法不正确的是( )
T℃下的溶液中,c(H+)=1.0×10-xmol?L-1,c(OH-)=1.0×10-ymol?L-1,x与y的关系如图所示.下列说法不正确的是( )| A、T℃时,水的离子积Kw为1×10-13 |
| B、T>25 |
| C、T℃时,pH=7的溶液显碱性 |
| D、T℃时,pH=12的苛性钠溶液与pH=1的稀硫酸等体积混合,溶液的pH=7 |
下列物质中含分子数目最多的是( )
| A、0.1mol Cl2 |
| B、0.4g H2 |
| C、4℃时9mLH2O |
| D、标况下,6.72L CO2 |