题目内容
下列关于各图象的解释或结论正确的是( )
A、.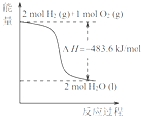 热化学方程式是H2(g)+
| ||
B、.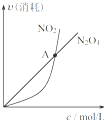 对于恒温恒容条件下的反应2NO2(g)?N2O4(g),A点为平衡状态 | ||
C、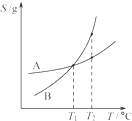 将A、B饱和溶液分别由T1℃升温至T2℃时,溶质的质量分数B>A | ||
D、.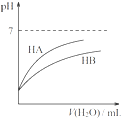 同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者 |
考点:反应热和焓变
专题:图示题
分析:A、图象中当放热483.6KJ时,是生成液态水的时候;
B、A点时,NO2和N2O4的消耗速率相等;
C、T1℃时,A和B的溶解度相同,溶质的质量分数相同;
D、酸越弱,其对应的盐越水解.
B、A点时,NO2和N2O4的消耗速率相等;
C、T1℃时,A和B的溶解度相同,溶质的质量分数相同;
D、酸越弱,其对应的盐越水解.
解答:
解:A、图象中当放热483.6KJ时,是生成液态水的时候,故热化学方程式应是H2(g)+
O2(g)=H2O(l)△H=-241.8 kJ/mol,故A错误;
B、A点时,只说明NO2和N2O4的消耗速率相等,而当NO2和N2O4的消耗速率之比为2:1时,反应才达平衡,故B错误;
C、T1℃时,A和B的溶解度相同,饱和溶液中溶质的质量分数相同,当升温到T2℃时,两者的溶解度均变大,无晶体析出,故溶液中的溶质的质量分数均不变,仍相等,故C错误;
D、从图象可以看出,加水稀释时,HA的pH变化大,故HA的酸性强于HB,而酸越弱,其对应的盐越水解,故同温度、同浓度的NaA溶液与NaB溶液相比,NaB的水解程度大,pH更大,其pH前者小于后者,故D正确;
故选D.
| 1 |
| 2 |
B、A点时,只说明NO2和N2O4的消耗速率相等,而当NO2和N2O4的消耗速率之比为2:1时,反应才达平衡,故B错误;
C、T1℃时,A和B的溶解度相同,饱和溶液中溶质的质量分数相同,当升温到T2℃时,两者的溶解度均变大,无晶体析出,故溶液中的溶质的质量分数均不变,仍相等,故C错误;
D、从图象可以看出,加水稀释时,HA的pH变化大,故HA的酸性强于HB,而酸越弱,其对应的盐越水解,故同温度、同浓度的NaA溶液与NaB溶液相比,NaB的水解程度大,pH更大,其pH前者小于后者,故D正确;
故选D.
点评:本题考查了图象的问题,应注意的是升高温度,A 和 B的溶解度均增大,无晶体析出,故溶质的质量分数不变.

练习册系列答案
相关题目
已知某温度下,Ksp(AgCl)=1.56×10-10 mol2?L-2,Ksp(Ag2CrO4)=1.12×10-12 mol3?L-3,下列叙述正确的是( )
| A、向氯化银的浊液中加入氯化钠溶液,氯化银的Ksp减小 |
| B、向2.0×10-4mol?L-1的K2CrO4溶液中加入等体积的2.0×10-4 mol?L-1 AgNO3溶液,则有Ag2CrO4沉淀生成 |
| C、将一定量的AgCl和Ag2CrO4固体混合物溶于蒸馏水中,充分溶解后,静置,上层清液中Cl-的物质的量浓度最大 |
| D、将0.001 mol?L-1的AgNO3溶液逐滴滴入0.001 mol?L-1的KCl和0.001 mol?L-1的K2CrO4的混合溶液中,则先产生AgCl沉淀 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、0.1mol Cl2与足量NaOH溶液反应,转移电子的数目为0.2NA |
| B、0.1mol苯乙烯中含有碳碳双键的数目为0.4NA |
| C、标准状况下,11.2L乙醇中含有羟基的数目为0.5NA |
| D、4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2NA |
下列属于放热反应的是( )
| A、浓硫酸的稀释 |
| B、铝热反应 |
| C、氢气还原氧化铜 |
| D、Ba(OH)2?2H2O和NH4Cl(固体)混合 |
下列有关化学用语表示正确的是( )
A、氮气的电子式: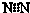 | ||
B、羟基的电子式: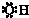 | ||
C、氯离子的结构示意图: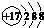 | ||
D、质子数为92、中子数为146的铀(U)原子的核素符号:
|
下列有关仪器使用方法或实验操作正确的是( )
| A、分液时下层液体从分液漏斗下端放出,上层液体从上口倒出 |
| B、酸碱滴定实验中,酸式滴定管装液前不必先用待装溶液润洗 |
| C、蒸馏过程中,冷却水从冷凝管的上端通入 |
| D、配制一定物质的量浓度的溶液时,直接将称取的固体药品倒入容量瓶加水溶解 |
