题目内容
请画出下列图形并解释其含意.
(1)1s态的界面示意图 .
(2)3dxy电子的几率密度的示意图 .
(3)3dz2轨道示意图 .
(1)1s态的界面示意图
(2)3dxy电子的几率密度的示意图
(3)3dz2轨道示意图
考点:原子核外电子排布,原子核外电子的运动状态
专题:原子组成与结构专题
分析:(1)1s态的原子轨道为球形,将电子云密集区(90%几率)称为原子轨道;
(2)第三能层数五个d轨道(dz2、dx2-y2、dxy、dyz、dxz)中,有四个形状都为十字梅花形,分别为:dx2-y2、dxy、dyz、dxz但方向不同,
3dxy电子的几率密度的示意图表示运动在3dxy原子轨道上电子出现的几率密度;
(3)3dz2是五个d轨道中形状与众不同的一个,轨道示意图为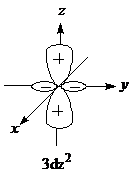 ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.
(2)第三能层数五个d轨道(dz2、dx2-y2、dxy、dyz、dxz)中,有四个形状都为十字梅花形,分别为:dx2-y2、dxy、dyz、dxz但方向不同,
3dxy电子的几率密度的示意图表示运动在3dxy原子轨道上电子出现的几率密度;
(3)3dz2是五个d轨道中形状与众不同的一个,轨道示意图为
 ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.解答:
解:(1)1s态的原子轨道为球形,球形区域内1s电子出现几率的90%,界面示意图为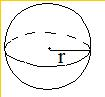 或
或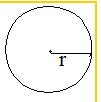 ,
,
故答案为: 或
或 ,以r为半径的球内1s电子出现的几率为90%;
,以r为半径的球内1s电子出现的几率为90%;
(2)第三能层数五个d轨道(dz2、dx2-y2、dxy、dyz、dxz)中,有四个形状都为十字梅花形,分别为:dx2-y2、dxy、dyz、dxz但方向不同,
3dxy电子的几率密度的示意图为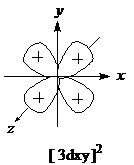 ,表示运动在3dxy原子轨道上电子出现的几率密度;
,表示运动在3dxy原子轨道上电子出现的几率密度;
故答案为: ,表示运动在3dxy原子轨道上电子出现的几率密度;
,表示运动在3dxy原子轨道上电子出现的几率密度;
(3)3dz2是五个d轨道中形状与众不同的一个,轨道示意图为 ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.
故答案为: ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.
 或
或 ,
,故答案为:
 或
或 ,以r为半径的球内1s电子出现的几率为90%;
,以r为半径的球内1s电子出现的几率为90%;(2)第三能层数五个d轨道(dz2、dx2-y2、dxy、dyz、dxz)中,有四个形状都为十字梅花形,分别为:dx2-y2、dxy、dyz、dxz但方向不同,
3dxy电子的几率密度的示意图为
 ,表示运动在3dxy原子轨道上电子出现的几率密度;
,表示运动在3dxy原子轨道上电子出现的几率密度;故答案为:
 ,表示运动在3dxy原子轨道上电子出现的几率密度;
,表示运动在3dxy原子轨道上电子出现的几率密度;(3)3dz2是五个d轨道中形状与众不同的一个,轨道示意图为
 ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.故答案为:
 ,描述了单个电子在3dz2运动时的状态函数图象.
,描述了单个电子在3dz2运动时的状态函数图象.
点评:本题考查了原子轨道的意义,难度一般,注意不同能级原子轨道的形状差异.

练习册系列答案
相关题目
如图是产生和收集气体的实验装置,该装置适合于( )
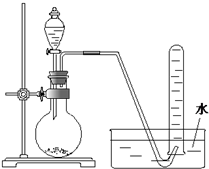

| A、用H2O2溶液和MnO2反应制取O2 |
| B、用浓盐酸和MnO2反应制取Cl2 |
| C、用稀硫酸与石灰石反应制取CO2 |
| D、用NH4Cl和Ca(OH)2反应制取NH3 |
将等质量的铜丝在酒精灯上加热后,分别插入下列物质中,放置片刻,铜丝质量增大的是( )
| A、硝酸 | B、无水乙醇 |
| C、氯化钠溶液 | D、盐酸 |
核外电子分层排布的主要原因是( )
| A、电子的质量不同 |
| B、电子的能量不同 |
| C、电子的数量不同 |
| D、电子的大小不同 |
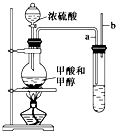 已知甲酸(HCOOH)是羧酸中组成最简单的酸,它具有羧酸的性质,在实验室里常用甲酸在浓硫酸的作用下制取少量一氧化碳,现用甲酸与甲醇反应制取甲酸甲酯来验证甲酸具有能发生酯化反应的性质,装置如图所示
已知甲酸(HCOOH)是羧酸中组成最简单的酸,它具有羧酸的性质,在实验室里常用甲酸在浓硫酸的作用下制取少量一氧化碳,现用甲酸与甲醇反应制取甲酸甲酯来验证甲酸具有能发生酯化反应的性质,装置如图所示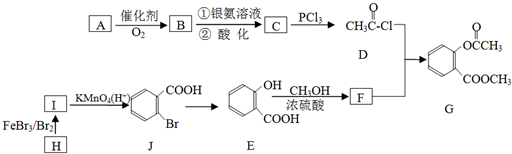
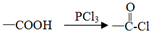
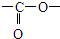 结构
结构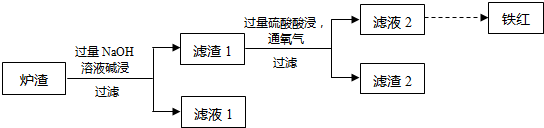
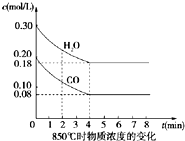 在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应:
在一体积为10L密闭的容器中,通入一定量的CO和H2O(g),在850℃时发生以下反应: