题目内容
1.有一包固体粉末,由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的三种物质组成,取样品进行如下实验,从实验可以判断( )
| A. | 该固体粉末中一定不含有BaCl2 | |
| B. | 该固体粉末中一定含有KNO3 | |
| C. | 它的组成可能是CaCO3、BaCl2、CuSO4 | |
| D. | 它的组成一定是CaCO3、Na2SO4、KNO3 |
分析 固体粉CaCO3、Na2SO4、KNO3、BaCl2、CuSO4溶于水分别为沉淀、无色溶液、无色溶液、无色溶液、蓝色溶液,依据题意能排除CuSO4;难溶物溶于稀盐酸,说明一定含有碳酸钙,硫酸钠和氯化钡不会同时存在,还有一种物质就是硝酸钾,据此回答.
解答 解:有一包固体粉末由CaCO3、Na2SO4、KNO3、BaCl2、CuSO4中的两种物质组成,取样品加水,出现白色沉淀,该白色沉淀能够溶于稀盐酸,则该固体粉末中一定含有CaCO3,且硫酸钠与氯化钡不会同时存在;得到无色溶液,该固体粉末中一定不含有CuSO4,因为CuSO4溶于水显蓝色;
综上得到:该固体粉末含有的三种物质可能为:CaCO3、Na2SO4、KNO3 或CaCO3、BaCl2、KNO3,
故选B.
点评 本题主要考查了几种未知物的检验,题目难度中等,注意掌握常见未知物检验的性质及检验方法.

练习册系列答案
相关题目
10.下列操作过程中,利用物质的氧化性的是( )
| A. | 明矾净化水 | B. | 纯碱除去油污 | ||
| C. | 臭氧用于餐具消毒 | D. | 食醋清洗水垢 |
7.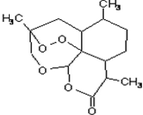 青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
 青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )| A. | 分子式是C15H22O5 | |
| B. | 易溶于水,乙醇和乙醚 | |
| C. | 含有-O-O-键,具有较强的氧化性 | |
| D. | 1mol青蒿素可以和1molH2发生加成反应 |
14.下列溶液中导电性最强的是( )
| A. | 1L0.1mol/L醋酸 | B. | 0.5L0.1mol/L氯化钠溶液 | ||
| C. | 0.1L0.1mol/L硫酸钠溶液 | D. | 2L0.1mol/L磷酸溶液 |
11.下列表示化学反应的离子方程式,其中正确的是( )
| A. | NH4HSO3溶液与足量NaOH溶液共热:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$ NH3↑+SO32-+2H2O | |
| B. | 向氯化铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | 用盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2 MnO4-+6H++5H2O2═2Mn2++5 O2↑+8H2O | |
| D. | 用石墨电极电解饱和MgCl2溶液:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+2OH- |
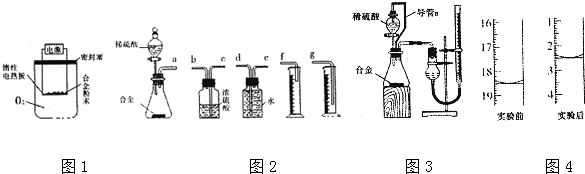
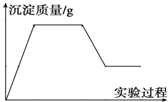 有一包白色固体物质,可能含有CuSO4、K2SO4、Na2CO3、Ca (NO3)2、KCl 中的一种或几种.将该白色固体少量溶于水中,得到无色透明溶液,取100mL该溶液先滴加足量硝酸钡溶液,再滴加足量稀硝酸,实验过程中沉淀质量的变化如图所示:
有一包白色固体物质,可能含有CuSO4、K2SO4、Na2CO3、Ca (NO3)2、KCl 中的一种或几种.将该白色固体少量溶于水中,得到无色透明溶液,取100mL该溶液先滴加足量硝酸钡溶液,再滴加足量稀硝酸,实验过程中沉淀质量的变化如图所示: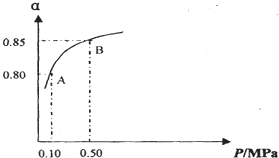
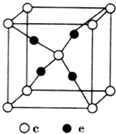 周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题: .
.