题目内容
在一定温度下的定容密闭容器中,当下列物理量不再变化时,表明反应:A(s)+2B(g)?C(g)+D(g)已达平衡的标志是( )
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、容器内B、C、D的浓度之比为2:1:1 |
| D、混合气体的总物质的量 |
考点:化学平衡状态的判断
专题:
分析:根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答:
解:A、反应前后气体体积不变,随着反应的进行体系压强不变,所以容器内压强保持不变,不一定达平衡状态,故A错误;
B、混合气体的密度不变,说明气体的质量不变,即正逆反应速率相等,故B正确;
C、平衡时容器内B、C、D的浓度之比决定于反应前加入各物质的多少,与是否平衡无关,故C错误;
D、反应体系中气体的物质的量是一定值,所以混合气体的总物质的量不变不一定平衡,故D错误;
故选B.
B、混合气体的密度不变,说明气体的质量不变,即正逆反应速率相等,故B正确;
C、平衡时容器内B、C、D的浓度之比决定于反应前加入各物质的多少,与是否平衡无关,故C错误;
D、反应体系中气体的物质的量是一定值,所以混合气体的总物质的量不变不一定平衡,故D错误;
故选B.
点评:本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等.

练习册系列答案
相关题目
X、Y、Z、W是原子序数依次增大的短周期主族元素,X、Z在周期表中的相对位置如下表.已知X元素最低负化合价的绝对值与其原子最外层电子数相等,Y是地壳中含量最多的金属元素.下列说法错误的是( )
| X | ||
| Z |
| A、X位于第二周期第ⅣA族 |
| B、原子半径由小到大的顺序为:W<Z<Y |
| C、Z、W两元素的气态氢化物中,Z的气态氢化物更稳定 |
| D、无论氧气是否过量,Z在氧气中燃烧的产物唯一 |
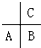 短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )
短周期元素A、B、C(均不为稀有气体元素)在周期表中的位置如图:下列说法正确的是( )| A、若均为非金属元素,其气态氢化物稳定性:A<B<C |
| B、若均为金属元素,其最高价氧化物的水化物的碱性:A<B<C |
| C、原子半径:A>C>B |
| D、最高正价:A>B>C |
下列事实与胶体性质无关的是( )
| A、在豆浆里加入盐卤做豆腐 |
| B、在河流入海处易形成沙洲 |
| C、“尿毒症”患者做血液透析治疗 |
| D、三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀 |
pH=13的 强碱与pH=2的强酸溶液混合,所得混合液的pH=7,则强碱与强酸的体积比为( )
| A、9:1 | B、1:9 |
| C、1:10 | D、10:1 |
 (1)现有以下物质①NaOH溶液 ②干冰 ③稀硫酸 ④铜 ⑤醋酸 ⑥BaSO4固体 ⑦蔗糖 ⑧食盐晶体 ⑨酒精 ⑩熔融的KNO3,其中属于电解质的是:
(1)现有以下物质①NaOH溶液 ②干冰 ③稀硫酸 ④铜 ⑤醋酸 ⑥BaSO4固体 ⑦蔗糖 ⑧食盐晶体 ⑨酒精 ⑩熔融的KNO3,其中属于电解质的是: