题目内容
5.甲、乙两密闭容器中均发生反应:C(s)+2H2O(g)?CO2(g)+2H2(g)△H>0,有关实验数据如下表所示,下列说法正确的是( )| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | 平衡常数 | |
| C(s) | H2O(g) | H2(g) | |||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | t1 | K1 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | t2 | K2 |
| A. | T1<T2 | |
| B. | 乙容器中,当反应进行到$\frac{{t}_{2}}{2}$min时,n(H2O)=1.4 mol | |
| C. | K2=1.35 mol•L-1(或K2=1.35) | |
| D. | 混合气体的密度始终保持不变 |
分析 A.该反应为吸热反应,由起始时甲中n(H2O)为乙中2倍,且平衡时甲中n(H2)大于乙中2倍,可知升高温度平衡正向移动;
B.由表格数据可知,若为平均速率时反应进行到$\frac{{t}_{2}}{2}$min,n(H2O)=2mol-0.6mol=1.4 mol,但开始时反应速率快;
C.C(s)+2H2O(g)?CO2(g)+2H2(g)
开始 2 0 0
转化 1.2 0.6 1.2
平衡 0.8 0.6 1.2
则K2=$\frac{\frac{0.6mol}{1L}×(\frac{1.2mol}{1L})^{2}}{(\frac{0.8mol}{1L})^{2}}$;
D.C为固体,平衡前混合气体的质量为变量,结合$ρ=\frac{m}{V}$分析.
解答 解:A.该反应为吸热反应,由起始时甲中n(H2O)为乙中2倍,且平衡时甲中n(H2)大于乙中2倍,可知升高温度平衡正向移动,则T1>T2,故A错误;
B.由表格数据可知,若为平均速率时反应进行到$\frac{{t}_{2}}{2}$min,n(H2O)=2mol-0.6mol=1.4 mol,但开始时反应速率快,则n(H2O)<1.4 mol,故B错误;
C.C(s)+2H2O(g)?CO2(g)+2H2(g)
开始 2 0 0
转化 1.2 0.6 1.2
平衡 0.8 0.6 1.2
则K2=$\frac{\frac{0.6mol}{1L}×(\frac{1.2mol}{1L})^{2}}{(\frac{0.8mol}{1L})^{2}}$=1.35 mol•L-1(或K2=1.35),故C正确;
D.碳为固体,平衡前混合气体的质量为变量,体积不变,则密度在平衡前为变量,故D错误;
故选C.
点评 本题考查化学平衡的计算,为高频考点,把握表格数据的应用、K的计算、平衡移动及判定为解答的关键,侧重分析与计算能力的考查,注意利用平衡浓度计算K,题目难度不大.

| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50 s的平均速率为v(PCl3)=0.0032mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入1.0molPCl5、0.20molPCl3和0.20molCl2,达到平衡前v(正)<v(逆) | |
| D. | 相同温度下,起始时向容器中充入2.0molPCl3、2.0molCl2,达到平衡时,PCl3的转化率大于80% |
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 1 | ① | ② | ||||||
| 2 | ③ | ④ | ⑤ | ⑥ | ||||
| 3 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)(填写元素符号)①H③C⑤O ⑦Na⑨S
(2)①和④号元素形成的化合物的化学式为NH3,用电子式表示其形成过程为3H•+
 →
→ .
.(3)⑦和⑧号元素的最高价氧化物的水化物的碱性是:NaOH>Mg(OH)2 (填化学式).
⑨和⑩号元素的最高价氧化物的水化物的酸性是:HClO4>H2SO4 (填化学式).
(4)①、⑤、⑦号元素形成的一种化合物的电子式是
 ,在该化合物中既含有离子键,又含有共价键.
,在该化合物中既含有离子键,又含有共价键. | A. | C3H7OH | B. | CH2O | C. | C2H6O | D. | C3H6O2 |

| A. | 4种 | B. | 8种 | C. | 16 种 | D. | 36 种 |
 ,ZX与水反应放出的气体的化学式为H2.
,ZX与水反应放出的气体的化学式为H2.


 +2H2O,其反应类型为酯化反应.
+2H2O,其反应类型为酯化反应. .
.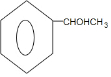 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$ +H2O.
+H2O. (填结构简式)
(填结构简式) 2C(g) △H=-QkJ/mol,保持其它条件不变,只改变起始加入量,测得相关数据如表所示:
2C(g) △H=-QkJ/mol,保持其它条件不变,只改变起始加入量,测得相关数据如表所示: