题目内容
(10分)实验室常用二氧化锰和浓盐酸反应制取氯气,反应式如下:
MnO2+ 4HCl(浓)=MnCl2+Cl2↑+2H2O
(1)用双线桥法表示上述反应中电子转移的方向和数目。
(2)反应中发生氧化反应的物质是___________(填化学式),被还原的元素是___________(填元素名称)。
(3)氧化剂与还原剂的物质的量之比为_________________。
(4)若反应中被氧化的盐酸为1mol,则生成的氯气体积为 (标准状况下)。
(10分)(1)

(2) HCl 锰
(3) 1﹕2
(4)11.2L
【解析】
试题分析:(1)MnO2+ 4HCl(浓)=MnCl2+Cl2↑+2H2O反应中,+4价Mn的化合价降低2价,得到2个电子,Cl元素的化合价整体升高2价,失去2个电子,所以用双线桥表示为
 ;
;
(2)在该反应中,Cl元素的化合价升高,被氧化,所以发生氧化反应的物质是HCl,Mn元素的化合价降低,被还原;
(3)参加反应的HCl中只有1/2被氧化,所以氧化剂与还原剂的物质的量之比为1:2;
(4)若反应中被氧化的盐酸为1mol,根据2HCl~Cl2,所以生成氯气的物质的量是0.5mol,标准状况下的体积是0.5mol×22.4L/mol=11.2L。
考点:考查对氧化还原反应的分析,双线桥的表示

练习册系列答案
相关题目
 2Z(g),若X、Y、Z的起始浓度分别为c
2Z(g),若X、Y、Z的起始浓度分别为c 、c
、c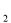 、c
、c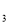 (均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是
(均不为零),到达平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是