题目内容
3.已知由CH4、C2H2、C2H4、C2H6四种气态烃中的某两种烃组成的混合气体0.1mol,完全燃烧得0.14molCO2和4.32gH2O,则这两种烃的物质的量之比可能为( )| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 2:5 |
分析 4.32g水的物质的量为:$\frac{4.32g}{18g/mol}$=0.24mol,即0.1mol混合烃完全燃烧生成0.14molCO2和0.24molH2O,根据元素守恒,则混合烃的平均分子式为C1.4H4.8,而碳原子数小于1.6的只有甲烷,则混合气体中一定含有CH4,根据氢原子平均数目可知另一种烃分子中含有H原子数越大大于4,则一定含有C2H6,设出甲烷和乙烷的物质的量,然后根据平均分子式列式计算即可.
解答 解:4.32g水的物质的量为:$\frac{4.32g}{18g/mol}$=0.24mol,即0.1mol混合烃完全燃烧生成0.14molCO2和0.24molH2O,根据元素守恒,则混合烃的平均分子式为C1.4H4.8,而碳原子数小于1.6的只有甲烷,则混合气体中一定含有CH4,根据氢原子平均数目可知另一种烃分子中含有H原子数越大大于4,则一定含有C2H6,
设CH4、C2H6的物质的量分别为x、y,
根据平均C原子数为1.4可知:$\frac{x+2y}{x+y}$=1.4,整理可得x:y=3:2,CH4、C2H6的物质的量之比为2:3时,平均H原子数=$\frac{4×3+6×2}{2+3}$=4.8,满足条件,即C2H6、CH4的物质的量之比为2:3,
故选C.
点评 本题考查混合物反应的计算,题目难度不大,根据质量守恒定律正确计算混合烃的平均分子式为解答关键,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
相关题目
20.H2(g)+I2(g)?2HI(g)△H=-Q(Q>0),下列说法正确的是( )
| A. | 温度升高,反应速率增大,产率增大 | |
| B. | 增大反应物H2的浓度,HI%增大 | |
| C. | 增大压强,浓度增大,平衡不移动 | |
| D. | 使用催化剂,反应速率增大,I2的转化率增大 |
18.自然界中的许多植物中含有醛,其中有些具有特殊香味,可作为植物香料使用,例如桂皮含肉桂醛(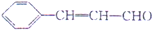 ),杏仁含苯甲醛(
),杏仁含苯甲醛(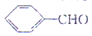 ).下列说法错误的是( )
).下列说法错误的是( )
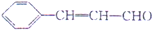 ),杏仁含苯甲醛(
),杏仁含苯甲醛(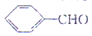 ).下列说法错误的是( )
).下列说法错误的是( )| A. | 肉桂醛和苯甲醛互为同系物 | |
| B. | 肉桂醛能发生加成反应、取代反应和加聚反应 | |
| C. | 可用新制氢氧化铜悬浊液检验肉桂醛分子中的含氧官能团 | |
| D. | 1mol肉桂醛分子在一定条件下最多与5mol氢气加成 |
5.在给定的条件下,下列选项所示的物质间转化均能一步实现的是( )
| A. | FeSO4(aq)$\stackrel{氢气}{→}$Fe$→_{高温}^{H_{2}O(g)}$Fe2O3 | |
| B. | Cu2S$→_{高温}^{O_{2}}$Cu$\stackrel{FeCl_{3}(aq)}{→}$CuCl2(aq) | |
| C. | Ca(OH)2$\stackrel{Cl_{2}}{→}$Ca(ClO)2$→_{H_{2}O}^{SO_{2}(足量)}$HClO | |
| D. | Fe2O3$\stackrel{HCl(aq)}{→}$FeCl3(aq)$\stackrel{△}{→}$无水FeCl3 |
8.苯乙烯的结构为 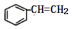 ,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有( )
,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有( )
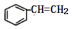 ,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有( )
,该物质在一定条件下能和氢气完全加成,加成产物的一溴取代物有( )| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
12.1mol酯R完全水解可得到l molC5H8O4和2mol甲醇,下列有关酯R的分子式和分子结构数目正确的是( )
| A. | C7H12O4,4种 | B. | C7H12O4,6种 | C. | C7H14O2,8 种 | D. | C7H14O2,10种 |
13.化学与科技、社会、生活有着密切的联系.下列有关说法正确的是( )
| A. | 用于消除H7N9病毒的漂白粉是一种强电解质 | |
| B. | 古代制盐(NaCl)有“东晒西煮”之说,是利用了复杂的物理、化学方法 | |
| C. | 铜带(镀锡)是光伏电池的电子元件,破损时不加快其腐蚀 | |
| D. | 纤维素、蛋白质和油脂均可发生水解,都属于天然高分子化合物 |
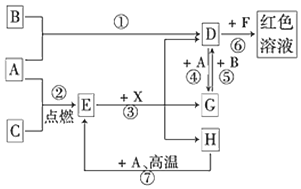
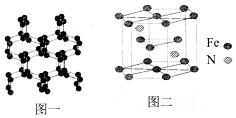 南京理工大学化工学院胡炳成教授团队于2017年1月成功合成世界首个全氮阴离子盐,使氮原子簇化合物的研究又有了新的突破.请根据材料回答以下问题:
南京理工大学化工学院胡炳成教授团队于2017年1月成功合成世界首个全氮阴离子盐,使氮原子簇化合物的研究又有了新的突破.请根据材料回答以下问题: .
.