题目内容
18.下列各组离子在指定溶液中,能大量共存的是( )①无色溶液中:K+、Cl-、Na+、SO42-
②使pH=11的溶液中:Na+、AlO2-、K+、CO32-
③水电离的c(H+)=10-12mo1/L的溶液中:Cl-、HCO3-、NH4+、SO32-
④加Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、SO32-
⑤酸性溶液中:Fe2+、Ag+、NO3-、I-.
| A. | ①②③④⑤ | B. | ①②⑤ | C. | ①② | D. | ①②③④ |
分析 ①该组离子之间不反应,且均为无色;
②pH=11的溶液,显碱性,该组离子之间不反应;
③水电离的c(H+)=10-12mo1/L的溶液,为酸或碱溶液;
④加Mg能放出H2的溶液,显酸性;
⑤酸性溶液中离子之间发生氧化还原反应,离子之间结合生成沉淀.
解答 解:①该组离子之间不反应,可大量共存,且均为无色,故正确;
②pH=11的溶液,显碱性,该组离子之间不反应,可大量共存,故B正确;
③水电离的c(H+)=10-12mo1/L的溶液,为酸或碱溶液,酸溶液中不能大量存在HCO3-、SO32-,碱溶液中不能大量存在HCO3-、NH4+,故错误;
④加Mg能放出H2的溶液,显酸性,不能大量存在SO32-,故错误;
⑤酸性溶液中Fe2+(或I-)、NO3-发生氧化还原反应,Ag+、I-结合生成沉淀,不能大量共存,故错误;
故选C.
点评 本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应、氧化还原反应的离子共存考查,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
3.用下列实验装置完成对应的实验(部分仪器已省),能达到实验目的是( )
| A. | 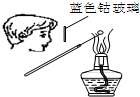 检验Na2CO3中的Na+ | B. | 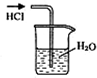 吸收HCl | ||
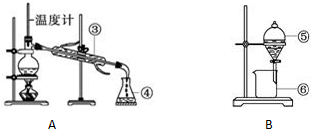
| C. | 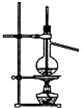 石油的蒸馏 | D. | 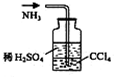 吸收NH3 |
7. 常温下,将氯气缓慢通入水中至饱和,再向其中缓慢滴加0.1 mol•L-1 NaOH溶液,整个过程中pH变化如图所示,下列有关叙述不正确的是( )
常温下,将氯气缓慢通入水中至饱和,再向其中缓慢滴加0.1 mol•L-1 NaOH溶液,整个过程中pH变化如图所示,下列有关叙述不正确的是( )
 常温下,将氯气缓慢通入水中至饱和,再向其中缓慢滴加0.1 mol•L-1 NaOH溶液,整个过程中pH变化如图所示,下列有关叙述不正确的是( )
常温下,将氯气缓慢通入水中至饱和,再向其中缓慢滴加0.1 mol•L-1 NaOH溶液,整个过程中pH变化如图所示,下列有关叙述不正确的是( )| A. | a点时,某同学用玻璃棒蘸取溶液滴在蓝色的石蕊试纸上,试纸最终变红 | |
| B. | a-b段,溶液中$\frac{c({H}^{+})}{c(Cl{O}^{-})}$增大 | |
| C. | b点对应溶液中:c(Cl-)>c(H+)>c(HClO)>c(ClO-)>c(OH-) | |
| D. | c点对应溶液中:c(Na+)=2c(ClO-)+c(HClO) |
12.下列图示过程,由太阳能直接转变为化学能的是( )
| A. | 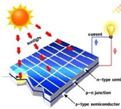 光伏发电 | B. |  风力发电 | C. |  水力发电 | D. | 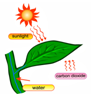 光合作用 |