题目内容
某氧化物不溶于水,与NaOH反应生成易溶于水的化合物M,在M溶液滴加稀盐酸中,有白色沉淀产生,则原氧化物是( )
| A、Fe2O3 | B、SiO2 | C、SO2 | D、MgO |
分析:A.氧化铁不能溶于烧碱;
B.二氧化硅能和碱反应生成硅酸盐,可溶性的硅酸盐滴入盐酸中生成硅酸沉淀;
C.二氧化硫和碱生成亚硫酸盐,在盐酸中不能生成沉淀;
D.氧化镁不能溶于烧碱;
B.二氧化硅能和碱反应生成硅酸盐,可溶性的硅酸盐滴入盐酸中生成硅酸沉淀;
C.二氧化硫和碱生成亚硫酸盐,在盐酸中不能生成沉淀;
D.氧化镁不能溶于烧碱;
解答:解:A.氧化铁不能溶于烧碱,故A错误;
B.二氧化硅可与氢氧化钠反应生成硅酸钠,硅酸钠滴入盐酸中生成白色的硅酸沉淀,故B正确;
C.二氧化硫与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与盐酸反应生成氯化钠、水和二氧化硫,故C错误;
D.氧化镁不能溶于烧碱,故D错误;
故选B.
B.二氧化硅可与氢氧化钠反应生成硅酸钠,硅酸钠滴入盐酸中生成白色的硅酸沉淀,故B正确;
C.二氧化硫与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与盐酸反应生成氯化钠、水和二氧化硫,故C错误;
D.氧化镁不能溶于烧碱,故D错误;
故选B.
点评:本题考查硅和二氧化硅的性质,题目难度不大,注意二氧化硫与氢氧化钠反应生成亚硫酸钠,亚硫酸钠与盐酸反应无沉淀.

练习册系列答案
相关题目
下表为元素周期表的一部分,参照元素①~⑦在表中的位置
请用相关的化学用语回答下列问题:
|
族 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
|
|
② |
④ |
|
|
3 |
⑤ |
|
③ |
|
|
⑥ |
⑦ |
|
(1)④、⑤、⑦的原子半径由大到小的顺序为___________。
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为_______>_______。
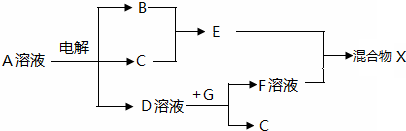
(3)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体。

① 写出D溶液与G反应的化学方程式__________________________________________。
② 写出检验A溶液中溶质的阳离子的方法: __________________________________。
③ 混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,请写出它在苛性钠溶液中发生反应的离子方程式_____________________________________。
下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用相关的化学用语回答下列问题:
(1)④、⑤、⑦的原子半径由大到小的顺序为______.
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为______>______.
(3)③元素的原子核外共有______种不同能级的电子,它们共填充了______个轨道.
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体.

①写出D溶液与G反应的化学方程式______.
②写出检验A溶液中溶质的阳离子的方法:______.
③混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,请写出它在碱性溶液中的电离方程式______.
| 族 周期 | IA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ||||||
| 3 | ⑤ | ③ | ⑥ | ⑦ | ||||
(2)⑥和⑦的最高价氧化物对应的水化物的酸性强弱为______>______.
(3)③元素的原子核外共有______种不同能级的电子,它们共填充了______个轨道.
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气体.

①写出D溶液与G反应的化学方程式______.
②写出检验A溶液中溶质的阳离子的方法:______.
③混合物X中的某物质不溶于水,但既能溶于酸又能溶于碱,请写出它在碱性溶液中的电离方程式______.