题目内容
下列反应的离子方程式书写正确的是( )
| A、过量二氧化碳与氢氧化钠溶液反应:CO2+OH-═CO32-+H2O |
| B、铁与稀硫酸反应;2Fe+6H+═2Fe3++3H2↑ |
| C、稀醋酸加入到氢氧化钡溶液中:H++OH-═H2O |
| D、氯气通入溴化钾溶液中:Cl2+2Br-═Br2+2Cl- |
考点:离子方程式的书写
专题:离子反应专题
分析:A.过量二氧化碳和氢氧化钠溶液反应生成碳酸氢钠;
B.稀硫酸具有弱氧化性,和铁反应生成亚铁盐;
C.弱电解质写化学式;
D.氯气和溴离子发生氧化还原反应生成溴.
B.稀硫酸具有弱氧化性,和铁反应生成亚铁盐;
C.弱电解质写化学式;
D.氯气和溴离子发生氧化还原反应生成溴.
解答:
解:A.过量二氧化碳和氢氧化钠溶液反应生成碳酸氢钠,离子方程式为CO2+OH-═HCO3-,故A错误;
B.稀硫酸具有弱氧化性,和铁反应生成亚铁盐,离子方程式为Fe+2H+═Fe2++H2↑,故B错误;
C.弱电解质写化学式,离子方程式为CH3COOH+OH-═H2O+CH3COO-,故C错误;
D.氯气和溴离子发生氧化还原反应生成溴,离子方程式为Cl2+2Br-═Br2+2Cl-,故D正确;
故选D.
B.稀硫酸具有弱氧化性,和铁反应生成亚铁盐,离子方程式为Fe+2H+═Fe2++H2↑,故B错误;
C.弱电解质写化学式,离子方程式为CH3COOH+OH-═H2O+CH3COO-,故C错误;
D.氯气和溴离子发生氧化还原反应生成溴,离子方程式为Cl2+2Br-═Br2+2Cl-,故D正确;
故选D.
点评:本题考查了离子方程式的正误判断,该题是高考中的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)、检查是否符合原化学方程式等.

练习册系列答案
相关题目
用CH4催化还原NOx可以消除氮氧化物的污染.例如:
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
下列说法不正确的是( )
①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ?mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ?mol-1
下列说法不正确的是( )
| A、由反应①、②可推知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H=-867 kJ?mol-1 |
| B、等物质的量的甲烷分别参与反应①、②,则反应转移的电子数相等 |
| C、若用标准状况下4.48 L CH4还原NO2至N2,放出的热量为173.4 kJ |
| D、若用标准状况下4.48 L CH4还原NO2至N2,整个过程中转移的电子总数为3.2NA |
下列化学式表示物质分子的是( )
| A、Na2SO4 |
| B、SiO2 |
| C、H2SO4 |
| D、Al |
下列说法中,正确的是( )
| A、常温常压下,22.4L O2含有的分子数目为NA |
| B、相同浓度的HCl与CH3COOH两溶液中c(H+)相同 |
| C、c(H+)>c(OH-)的溶液一定显碱性 |
| D、浓度均为0.10 mol?L-1的NH3?H2O和NH4Cl溶液等体积混合后:c(NH3?H2O)+c(NH4+)<0.20 mol?L-1 |
下列各物质中,能形成顺反异构体的是( )
| A、1-丁烯 |
| B、丙烯 |
| C、2-甲基-2-丁烯 |
| D、2,3-二氯-2-丁烯 |
下列化学用语表示正确的是( )
A、水的电子式: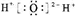 |
| B、乙烷的结构简式:C2H6 |
C、铝的原子结构示意图: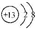 |
| D、硫酸钠的电离方程式:Na2SO4=2Na++SO42- |
下列物质不属于醛类的是( )
A、 |
B、 |
| C、CH2═CH-CHO |
| D、CH3-CH2-CHO |